De la microbiologie pour ceux qui ont les crocs
Un opportuniste de la peau.
Les avancées de la recherche sur le microbiote humain, comprenant les milliards de microbes qui vivent en nous et sur nous, ont changé la façon dont les scientifiques et les cliniciens comprennent le développement et la progression de nombreuses maladies humaines. La peau ne fait pas exception. Les scientifiques découvrent maintenant les microbes composant une peau saine, comment ces microbes assurent des fonctions essentielles à nos cellules cutanées et à notre système immunitaire, et surtout, comment leurs partenariats sont perturbés et deviennent hostiles dans diverses maladies de la peau.
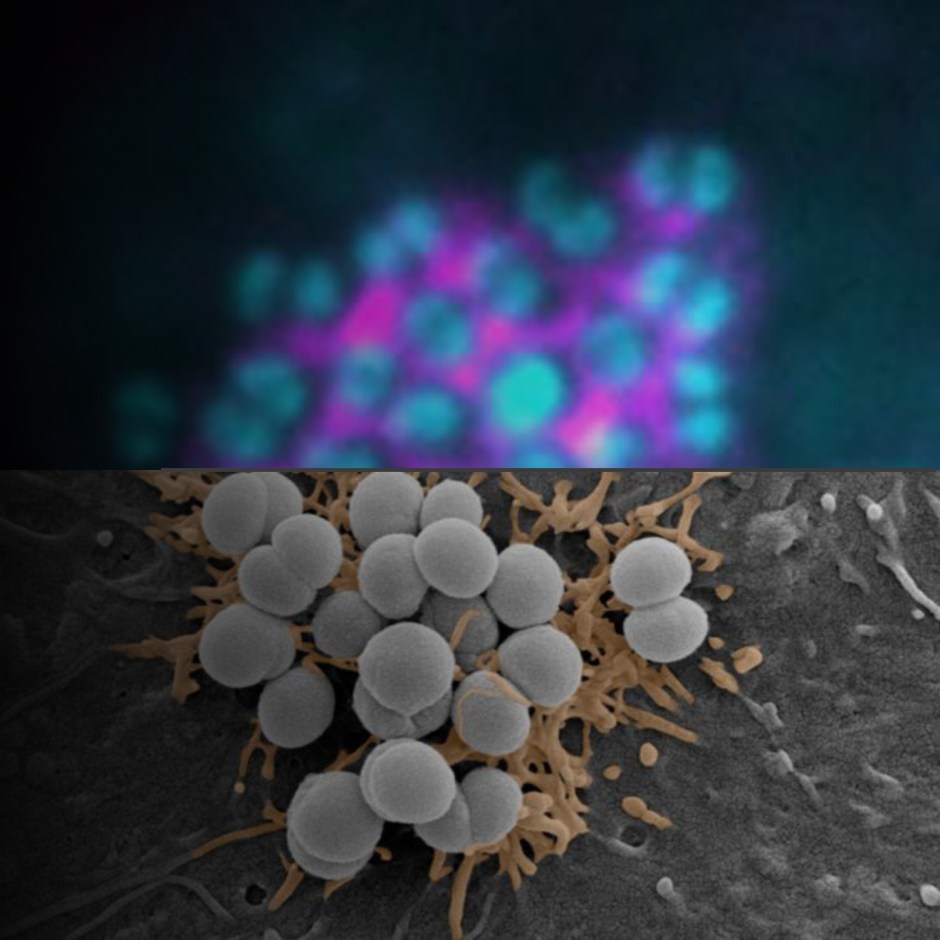
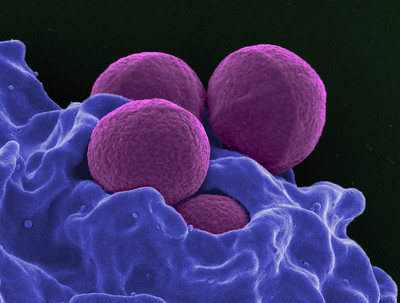
La dermatite atopique, communément appelée eczéma, est une maladie inflammatoire commune de la peau (1), une peau chroniquement enflammée, rouge, qui démange et sèche. Les causes profondes de l’eczéma ne sont pas claires et sont probablement une conséquence de l’interaction complexe entre notre génétique, notre environnement, notre fonction immunitaire et les microbes cutanés. Le microbe au centre de l’attention des pathologistes de l’eczéma est Staphylococcus aureus (2). Cependant, des recherches récentes ont révélé que Staphylococcus epidermidis, un microbe communement trouve sur notre peau, pourrait amplifier la gravité de cette maladie (3). S. epidermidis est généralement considéré comme un élément crucial d’une peau saine, et il l’est. Cependant, S. epidermidis est peut-être comme le Jekyll et Hyde microbien : dans certains cas, le symbiote protège contre les infections cutanées sévères et, en général, profite à l’homéostasie et à l’intégrité de la peau. En revanche, dans d’autres cas, il peut exacerber la rupture de la barrière cutanée (4). Un défi persistant sur le terrain consiste à identifier les environnements qui favorisent le commensalisme de S. epidermidis par rapport à la pathogénicité de S. epidermidis.
Dans une étude récente, les chercheurs ont affiné l’hypothèse selon laquelle, chez les patients atteints d’eczéma, S. epidermidis fabrique des molécules qui endommagent la peau (3). Plus précisément, ils ont examiné le rôle des protéases, des enzymes extracellulaires qui mâchent les protéines. Ils ont identifié une protéase appelée EcpA, dont ils ont découvert qu’elle pouvait dégrader une protéine essentielle de la barrière cutanée et un antimicrobien produit par la peau. Pour tester la capacité d’EcpA à perturber la barrière épidermique, les chercheurs ont colonisé la peau de souris avec deux souches distinctes de S. epidermidis : une qui produit l’EcpA et l’autre non. Seule la souche de S. epidermidis qui a produit l’EcpA pouvait pénétrer la barrière cutanée et provoquer des lésions cutanées. En effet, l’application de protéine EcpA purifiée directement sur la peau de souris a entraîné une perturbation similaire de la barrière cutanée, impliquant un rôle direct de l’EcpA dans l’exacerbation de la dégradation de la barrière.

Fait intéressant, le gène qui code pour EcpA est présent dans les souches commensales et pathogènes de S. epidermidis, ce qui suggère qu’il pourrait y avoir des conditions spécifiques qui permettent la virulence médiée par EcpA. Premièrement, les chercheurs observent que tous les S. epidermidis ne produisent pas d’EcpA au même niveau. Ainsi, la diversité au niveau de la souche, en particulier en termes d’expression d’EcpA, pourrait être une signature clé pour prédire la progression de la maladie. Deuxièmement, l’expression d’EcpA est régulée par un processus de signalisation bactérien appelé quorum sensing. Le quorum sensing est un type de communication entre cellules qui permet aux bactéries de recenser la densité et la composition de leur communauté proche et de coordonner leur expression génetique en conséquence. Dans ce cas, à haute densité cellulaire de S. epidermidis, la production d’EcpA s’accélère. La ramification de ceci est que EcpA est exprimé au maximum dans les communautés microbiennes de la peau qui abritent une prolifération de S. epidermidis. Les résultats de cette étude indiquent que les dommages cutanés chez les patients atteints d’eczéma pourraient être intensifiés par des souches de S. epidermidis qui produisent naturellement plus d’EcpA, et des conditions de communauté déséquilibrées (c’est-à-dire une abondance élevée de S. epidermidis) qui favorisent l’expression de cette protéine délétère.

Notre microbiome cutané fonctionne sur un système délicat de freins et contrepoids. Faire pencher la balance dans une direction (c’est-à-dire, trop d’une espèce bactérienne, trop peu d’une autre, un déclin de la diversité des espèces) pourrait faire des ravages sur les fonctions normales de la peau et attiser les réponses immunitaires. En effet, le déséquilibre microbien, ou dysbiose, est un fil conducteur parmi de nombreuses maladies inflammatoires. Comme indiqué, les moteurs de l’eczéma sont multiformes et complexes. Maintenant que les scientifiques découvrent comment S. epidermidis pourrait être virulent dans les cas d’eczéma, la prochaine étape consiste à identifier comment des facteurs supplémentaires (peut-être, génétiques ou environnementaux) fusionnent pour faciliter l’environnement idéal pour la pathogénicité de S. epidermidis.
Bien que l’apparition et la gravité de l’eczéma ne puissent pas être uniquement attribuées à S. epidermidis, l’identification d’agents spécifiques de lésions cutanées, comme l’EcpA, pourrait éclairer des approches plus sélectives et personnalisées du traitement et de la gestion des symptômes qui n’interfèrent pas avec la fonction immunitaire de l’hôte. Par exemple, des médicaments innovants pourraient s’opposer au quorum sensing de S. epidermidis pour inhiber la production d’EcpA. Il a déjà été démontré que les molécules anti-quorum sensing diminuent l’inflammation et les dommages cutanés provoqués par S. aureus (5). En revanche, les traitements de l’eczéma existants sont les corticostéroïdes à large spectre et d’autres immunosuppresseurs (6), qui atténuent la réponse immunitaire de l’hôte. Les inconvénients de ces médicaments sont qu’ils ne traitent pas la dysbiose microbienne et qu’ils pourraient conférer de graves effets secondaires à notre physiologie globale à long terme (7). Peut-être que se concentrer sur les composants microbiens des maladies de la peau pourrait devenir un pilier du développement futur de thérapies sûres et efficaces. Plus largement, la connaissance de la façon dont l’homéostasie microbienne est établie (et perturbée) pourrait lancer de nouvelles approches pour les soins standard et le maintien d’une peau saine.
References:
6. Plant A, Ardern-Jones MR. Advances in atopic dermatitis. Clin Med. 2021 May 17;21(3):177–81.
Image: https://www.wannapik.com/vectors/28885
Traduit par: Anaïs Biclot