De la microbiologie pour ceux qui ont les crocs
Une course aux armements entre le SARS-CoV-2 et notre système immunitaire
Les coronavirus sont une famille de virus qui provoquent depuis des décennies des maladies respiratoires et intestinales légères à graves chez l’homme et l’animal. La plupart des coronavirus humains provoquent le rhume, mais certains types, comme le SARS (syndrome respiratoire aigu sévère) et le MERS (syndrome respiratoire du Moyen-Orient), ont provoqué des flambées et des épidémies en 2002/2003 et 2012, respectivement. Le coronavirus le plus récent qui a créé des ravages à l’échelle mondiale et affecté la vie de chacun d’une manière ou d’une autre depuis son identification initiale en 2019 est le SARS-CoV-2. À l’instar de ses prédécesseurs, le SARS et le MERS, le SARS-CoV-2 est capable de provoquer une maladie grave avec divers impacts sanitaires à long terme qui ne sont pas entièrement compris.
L’émergence d’un nouveau coronavirus et notre incapacité à contrôler sa propagation rapide n’étaient pas notre seule préoccupation. Toutes les deux semaines ou tous les deux mois, nous entendons parler de nouveaux variants présentant des profils de maladie et de transmissibilité différents de ceux du SARS-CoV-2 original. Cela soulève la question suivante : dans quelle mesure sommes-nous protégés contre ces nouveaux variants ?
Que sont les variants du COVID-19 et comment apparaissent-ils ?
Au cours de la réplication virale, le génome viral peut acquérir des mutations génétiques aléatoires (qui sont des erreurs de copie du génome). Ce processus se produit constamment et est très avantageux pour le virus, car les mutations lui permettent de s’adapter à son environnement, de passer d’une espèce hôte à une autre et d’échapper aux mécanismes antiviraux exercés par notre système immunitaire. Ces mutations pourraient permettre au virus de devenir plus transmissible ou capable de provoquer des versions sévères de la maladie.
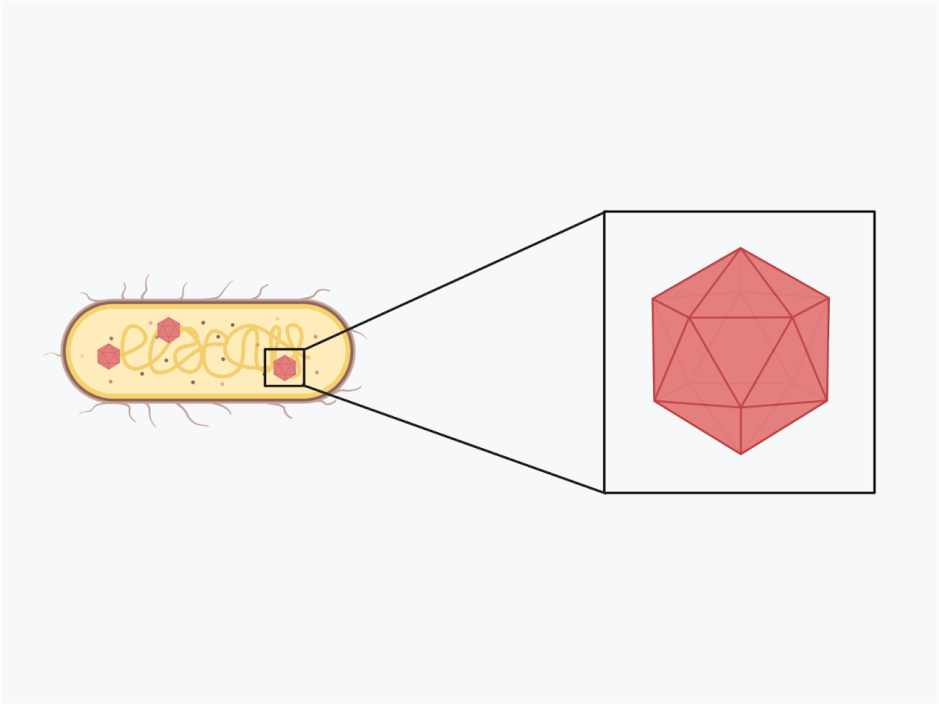
Les mutations de la protéine spike du SARS-CoV-2 (figure 1) sont particulièrement importantes. Il s’agit de la région du virus qui reconnaît et se lie aux récepteurs de la cellule hôte, et qui déclenche donc l’infection. De plus, comme la protéine spike est la partie la plus externe du virus et également la région virale codée par les vaccins covid, les systèmes immunitaires des hôtes précédemment infectés ou vaccinés peuvent facilement reconnaître la protéine spike originale. Par conséquent, des mutations dans cette région pourraient entraver la capacité du système immunitaire à reconnaître le virus.
Bien que ce processus produise continuellement de nouveaux variants, la plupart d’entre eux ne sont pas très préoccupants et ne persistent pas longtemps dans la population. Mais certains variants, comme Delta et Omicron, peuvent avoir un taux de transmission accru, provoquer une maladie plus grave ou avoir un impact sur l’efficacité des traitements et des vaccins. Ces variants sont classés comme Variants préoccupants (VoC – variant of concern en anglais).
L’exposition aux premiers variants de COVID-19 offre-t-elle une protection contre les nouveaux variants, comme Omicron ?
Gao et al. (2022) ont cherché à répondre à cette question en relation avec le variant omicron qui présente une transmissibilité accrue en raison de mutations de la protéine spike permettant une affinité de liaison plus élevée pour son récepteur hôte. De nombreux rapports et des données récentes indiquent que les anticorps neutralisants produits contre le SARS-CoV-2 original (figure 2b), par infection ou vaccination, sont beaucoup moins efficaces contre le variant omicron, peut-être en raison d’une moindre capacité à le reconnaître. Malgré cela, la plupart des personnes n’ont pas développé de maladie grave, ce qui suggère que d’autres zones du système immunitaire reconnaissent encore le virus et assurent une certaine protection contre lui.
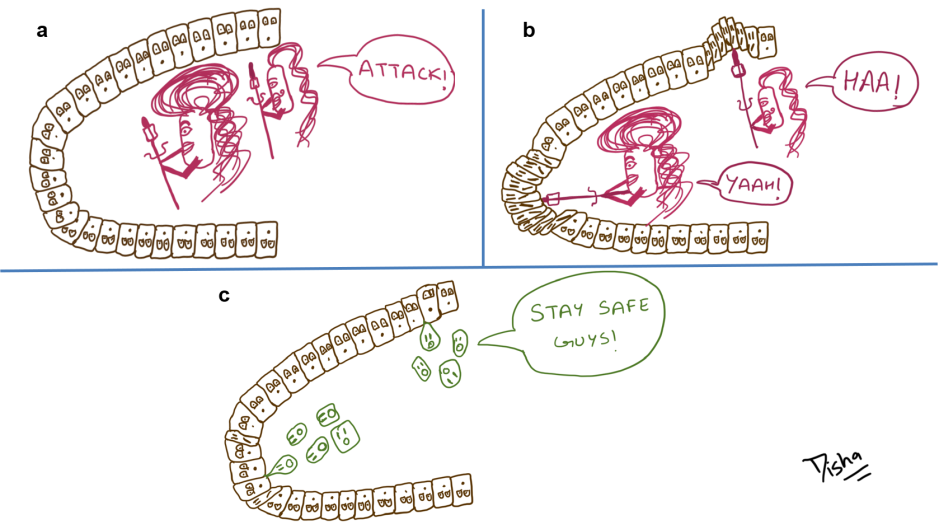
Outre les anticorps neutralisants, des données antérieures suggèrent également que les infections ou la vaccination contre le SARS-CoV-2 produisent également de fortes réponses des lymphocytes T qui peuvent également entraver la réplication du virus et la gravité de la maladie (figure 2a). Il est donc possible que les réponses des lymphocytes T générées contre le virus d’origine soient encore efficaces contre l’Omicron et le développement de la maladie grave.
Alors que les anticorps neutralisants se lient aux particules virales et empêchent ensuite le virus d’infecter nos cellules, la réponse des lymphocytes T cible les cellules déjà infectées par le virus et tue les cellules infectées (figure 2a). Une fois que le virus a infecté une cellule hôte, celle-ci traite de petites parties du virus (comme la protéine spike) et les affiche à sa surface à l’aide de molécules du complexe majeur d’histocompatibilité (CMH). En affichant une partie du virus à leur surface, ces cellules infectées signalent aux cellules immunitaires environnantes, telles que les lymphocytes T, qu’elles ont été infectées. Les lymphocytes T spécifiques de cette partie du virus sont alors capables de reconnaître le complexe CMH-antigène, puis de déclencher leur réponse “meurtrière”.
L’étude récente de Gao et al. (2022) a cherché à répondre à cette question en comparant l’activation spécifique de la protéine spike des cellules mononucléaires du sang périphérique – certains de vos globules blancs – dans trois groupes : 1) des individus doublement vaccinés avec Pfizer, 2) des individus convalescents qui avaient une infection légère ou sévère et 3) des individus non vaccinés et non infectés. Grâce à leurs expériences, ils ont observé que la réponse des lymphocytes T spécifiques de la protéine spike contre omicron était significativement plus faible, bien qu’il y ait une certaine réponse, dans le groupe des individus convalescents par rapport à la réponse contre la protéine spike originale. Cependant, le groupe de personnes vaccinées présentait une réponse cellulaire T similaire contre les protéines omicron et spike originales.
Globalement, ces résultats suggèrent que les réponses des lymphocytes T produites contre le variant original du SARS-CoV-2 par l’infection ou la vaccination peuvent reconnaître le variant omicron. Toutefois, les infections antérieures confèrent une protection relativement plus faible contre omicron par rapport aux personnes doublement vaccinées avec les vaccins Pfizer. Bien que ces résultats fournissent un aperçu intéressant de la protection immunitaire contre les nouveaux variants, il faut tenir compte du fait qu’ils ont été obtenus en comparant un petit nombre de sujets et que d’autres variables confusionnelles ont pu influencer les résultats. En outre, l’étude n’a porté que sur les échantillons de sang périphérique, qui fournissent des informations précieuses, mais ne sont pas une représentation complète de la réponse immunitaire totale exercée par notre organisme.
Article original Gao, Y., Cai, C., Grifoni, A. et al. Ancestral SARS-CoV-2-specific T cells cross-recognize the Omicron variant. Nat Med (2022).
Autres sources
- Centers for Disease Control and Prevention. (n.d.). SARS-COV-2 variant classifications and definitions. Centers for Disease Control and Prevention. Retrieved February 7, 2022, from https://www.cdc.gov/coronavirus/2019-ncov/variants/variant-classifications.html#anchor_1632154493691
- Centers for Disease Control and Prevention. (n.d.). Omicron variant: What you need to know. Centers for Disease Control and Prevention. Retrieved February 7, 2022, from https://www.cdc.gov/coronavirus/2019-ncov/variants/omicron-variant.html
- Callaway, E. (2021). Beyond omicron: What’s next for Covid’s viral evolution. Nature, 600(7888), 204–207. https://doi.org/10.1038/d41586-021-03619-8
Featured image: https://pixabay.com/vectors/corona-covid-19-coronavirus-virus-4942823/