De la microbiologie pour ceux qui ont les crocs
Les dommages collatéraux des antibiotiques.
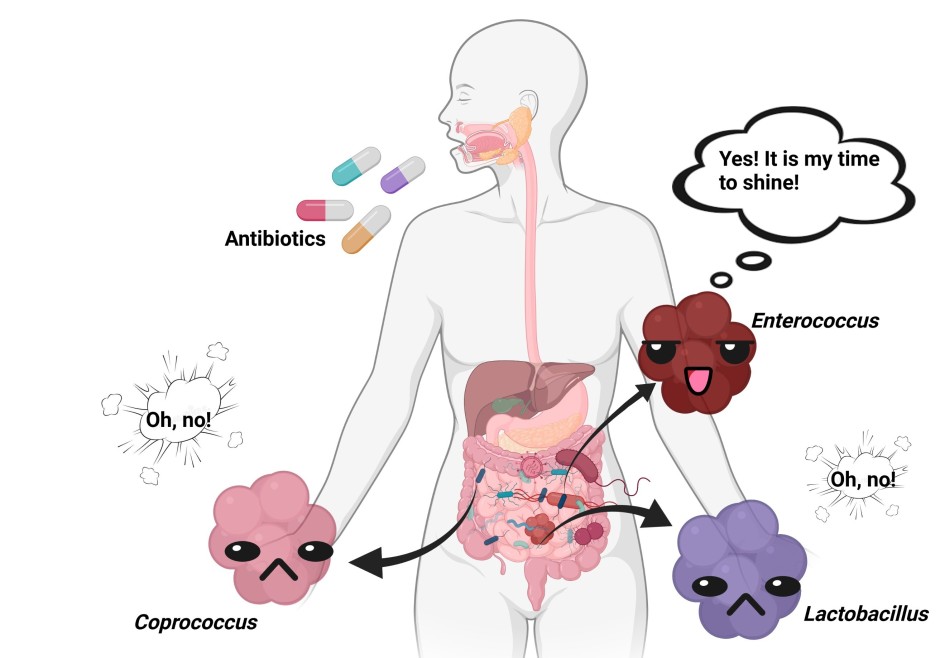
Les antibiotiques sont des médicaments puissants utilisés pour combattre les infections bactériennes. Cependant, les traitements antibiotiques peuvent également avoir un impact négatif sur notre microbiote intestinal, ce qui peut avoir des conséquences durables sur notre santé. Une étude publiée dans la revue Nature le mois dernier a examiné l’effet des antibiotiques couramment utilisés sur le microbiote intestinal humain et propose une stratégie pour atténuer les effets secondaires négatifs des antibiotiques sur ce dernier.
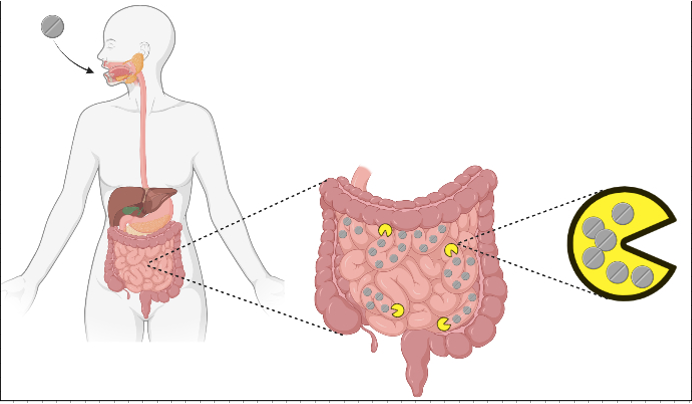
Notre intestin abrite des milliards de micro-organismes qui nous aident à digérer nos aliments, à produire des vitamines et des minéraux importants et à combattre les bactéries et les virus nuisibles. Les antibiotiques, bien qu’importants pour traiter des infections bactériennes potentiellement mortelles, peuvent perturber les communautés microbiennes de notre intestin. Ce déséquilibre peut entraîner des infections intestinales récurrentes causées par Clostridium difficile, caractérisées par une diarrhée sévère. Les modifications du microbiote intestinal dues aux antibiotiques peuvent également entraîner des troubles métaboliques ou immunologiques à long terme, comme l’obésité, les allergies ou l’asthme. Mais quels antibiotiques affectent quelles espèces bactériennes et comment ? Et comment atténuer ces effets secondaires négatifs ?
Le prix à payer
Pour mieux comprendre les “dommages collatéraux” des traitements antibiotiques, une équipe de recherche internationale dirigée par des scientifiques de l’EMBL Heidelberg et de l’université de Tübingen en Allemagne a entrepris de caractériser systématiquement les effets d’un large éventail d’antibiotiques sur les espèces bactériennes provenant de l’intestin humain. Les chercheurs ont suivi la croissance de 27 espèces bactériennes différentes après un traitement avec 144 antibiotiques différents. Ils ont également déterminé la concentration minimale inhibitrice (CMI) – la concentration minimale d’un antibiotique nécessaire pour inhiber la croissance bactérienne – pour plus de 800 de ces combinaisons antibiotique-bactérie.
Les scientifiques ont constaté que la majorité des bactéries intestinales avaient une CMI légèrement supérieure à celle des bactéries pathogènes, ce qui est une bonne nouvelle : avec concentrations d’antibiotiques utilisées en clinique, la plupart des bactéries intestinales testées n’étaient pas affectées. Toutefois, ce n’était pas le cas pour les tétracyclines, une classe d’antibiotiques largement utilisée. Les tétracyclines affectaient la croissance des bactéries intestinales à des concentrations bien inférieures à celles requises pour inhiber les bactéries pathogènes. En outre, les chercheurs ont constaté que les tétracyclines et les macrolides, une autre classe d’antibiotiques largement utilisée, non seulement inhibaient la croissance bactérienne, mais tuaient également plus de la moitié des espèces de bactéries intestinales testées. “Nous ne nous attendions pas à observer cet effet avec les tétracyclines et les macrolides, car ces classes d’antibiotiques étaient considérées comme n’ayant que des effets bactériostatiques – ce qui signifie qu’elles arrêtent la croissance bactérienne, mais ne tuent pas les bactéries”, a déclaré Camille Goemans, une autrice de l’étude. Ces effets bactéricides des tétracyclines et des macrolides pourraient tuer des membres spécifiques de notre microbiote intestinal, altérant ainsi sa composition pour une période potentiellement longue.
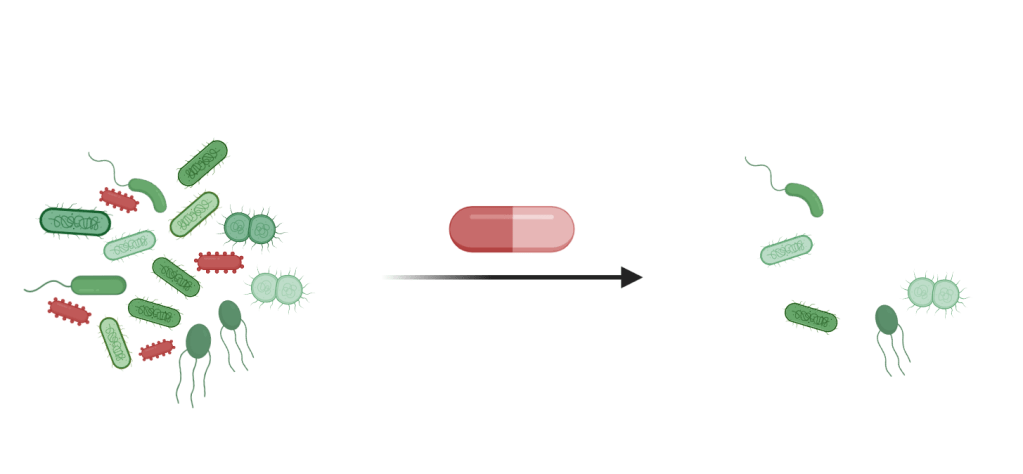
Un prix que nous n’avons pas à payer
Comment pouvons-nous réduire les dommages collatéraux des antibiotiques sur notre microbiote intestinal ? Un second médicament pourrait-il protéger les bactéries intestinales ? Les chercheurs ont passé en revue plus de 1 100 produits pharmaceutiques afin de trouver un antidote approprié qui protégerait deux espèces bactériennes intestinales abondantes contre les antibiotiques érythromycine, un macrolide, ou doxycycline, une tétracycline. Ils ont identifié quatre candidats prometteurs : le dicumarol, un anticoagulant, le benzbromarone, un médicament contre la goutte, et deux anti-inflammatoires, l’acide tolfénamique et le diflunisal. Fait important, ces médicaments n’ont pas interféré avec l’efficacité des antibiotiques contre les bactéries pathogènes. Ces antidotes n’ont pas seulement permis de protéger des espèces bactériennes intestinales isolées contre les deux antibiotiques ; ils ont également protégé des espèces bactériennes spécifiques dans des communautés microbiennes synthétiques, ainsi que dans des communautés bactériennes naturelles provenant d’échantillons de selles humaines et de souris vivantes. Ces résultats prometteurs ouvrent une possibilité intéressante d’atténuer les dommages collatéraux des antibiotiques.
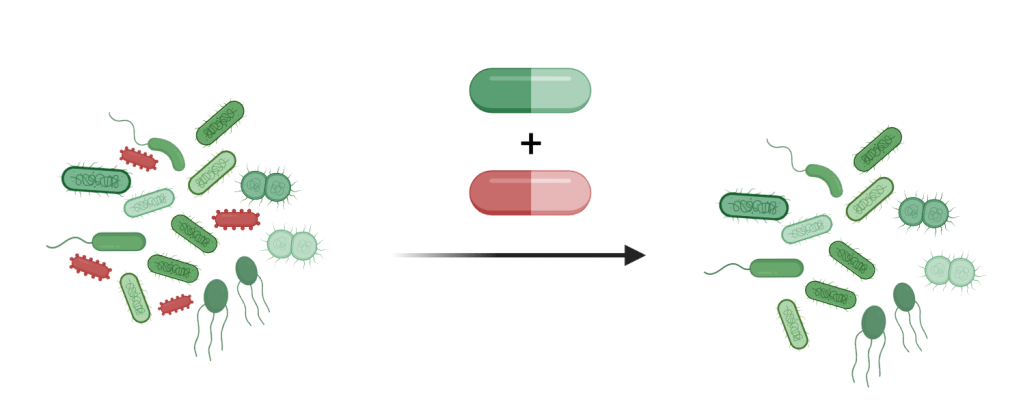
Avant de commencer à combiner les antibiotiques avec d’autres médicaments pour atténuer les dommages collatéraux des antibiotiques, des recherches supplémentaires sont nécessaires. Les antidotes eux-mêmes sont des médicaments qui ont leurs propres effets secondaires potentiels. Ainsi, la dose optimale d’un antidote doit être soigneusement définie pour minimiser les effets secondaires tout en maintenant une efficacité élevée. En outre, aucun antidote ne pourra à lui seul protéger l’ensemble de notre microbiote intestinal. Des combinaisons optimales et personnalisées d’antidotes doivent être définies. Nous commençons seulement à comprendre les interactions complexes entre les antibiotiques et notre microbiote intestinal. Cela nous permettra de trouver de nouveaux moyens de réduire le prix que nous payons pour les traitements antibiotiques.
Link to the original post: Maier, L., Goemans, C.V., Wirbel, J. et al. Unravelling the collateral damage of antibiotics on gut bacteria. Nature (2021).
Featured image: Image by Pete Linforth from Pixabay
Traduit par Anaïs Biclot