Microbiologie in hapklare porties
Je kan de pleuris krijgen! Maar waarom?
Tuberculose schrijft geschiedenis
De pleuris, de vliegende tering, de witte pest: allemaal namen voor een van de snelst verspreidende en dodelijkste ziektes ter wereld. De aandoening tuberculose wordt veroorzaakt door de bacterie Mycobacterium tuberculosis (MTB). MTB veroorzaakt celsterfte en neemt daarbij langzaam al het gezonde weefsel over. Tuberculose bestaat al zeker 6000 jaar en zorgt in ontwikkelingslanden nog steeds voor veel problemen. De ziekte eiste 1,4 miljoen slachtoffers in 2019 (Wereldgezondheidsorganisatie), dat maakte het de meest dodelijke besmettelijke ziekte. Alleen COVID-19 kon dat later nog overschaduwen. De behandeling voor tuberculose bestaat uit een zes tot achttien maand durende intensieve medicatiekuur, die nog eens lastiger wordt als je een multiresistente stam van MTB oppikt. Hoe krijgt de bacterie het voor elkaar om zo ongrijpbaar te zijn?
Het belangrijkste wapen van de hele familie Mycobacterium is de unieke celwand, die uit mycolzuren bestaat. Deze zuren zorgen voor een extreem harde celwand, die de bacterie beschermt tegen uitdroging, chemische schade en antibiotica. Hierdoor kunnen Mycobacteriën lange perioden binnen én buiten gastheren overleven. MTB kan zelfs overleven nadat het is “opgegeten” door macrofagen (onze immuuncellen die gespecialiseerd zijn in het afbreken van indringers). Sterker nog, de bacterie kan deze macrofagen zelfs als gastheercel gebruiken.
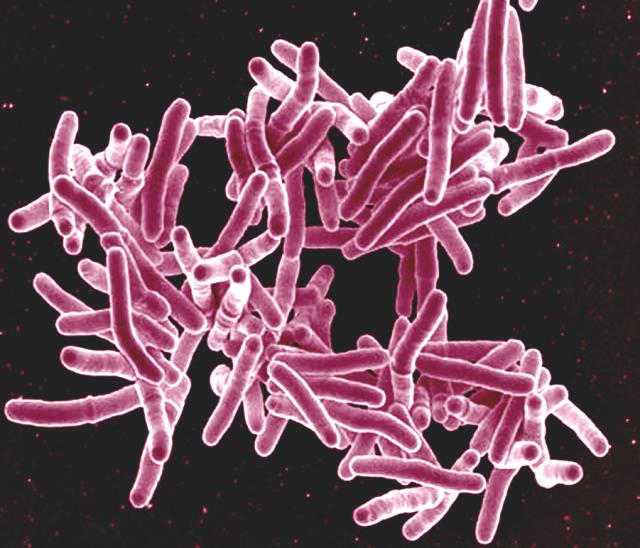
Stukbijten op Tuberculose
MTB kan de meeste aanvallen van macrofagen afslaan of ontwijken. Onze macrofagen werken volgens een twee-staps methode, die MTB kan verstoren. Eerst “eet” een macrofaag een indringer en sluit deze op in een speciaal organel, het fagosoom. De indringer zit hierin gevangen. Daarna zoekt het fagosoom een organel dat gevuld is met zuren en enzymen om de indringer kapot te maken (het lysosoom). Die twee organellen fuseren in een gezonde situatie tot één bacterie-gevangenis met verwoestende enzymen – maar niet als het aan MTB ligt! Deze bacterie scheidt eiwitten uit die het rekruteren van het lysosoom verhinderen, én onderdrukt de genen van de macrofaag die daarvoor nodig zijn. Als de macrofaag er toch in slaagt om de twee organellen bij elkaar te brengen, kan MTB zijn aanvaller zo saboteren dat het geen zuren kan inzetten als wapen. Zo kan MTB overleven en gedijen ín ons immuunsysteem.
Als een macrofaag een indringer niet aankan, heeft het twee opties. Ten eerste kan de macrofaag kiezen om zichzelf af te bouwen (apoptose). Zo komt de bacterie weer vrij, maar heeft het ook geen gastheer-cel meer en wordt dus in zijn groei geremd. Ten tweede kunnen macrofagen een granuloom maken: dat is een klomp van macrofagen waarin de bacterie gevangen wordt, en op die manier niet meer de rest van het lichaam kan infecteren [1]. Je voelt het al aankomen: de McGyver-bacterie MTB weet zich ook hieruit te worstelen door een proces dat “verkazing” wordt genoemd. De bacteriën eten zich een weg door de klompjes macrofagen en laten weefsel achter dat (volgens chirurgen) op gatenkaas lijkt.
Hiding in Plain Sight
https://live.staticflickr.com/7004/6545181037_e964e63448_b.jpg
De kern van zo’n granuloom bevat dode macrofagen en groeit totdat het granuloom barst. Dat gebeurt meestal wanneer het immuunsysteem van de gastheer verzwakt door iets in zijn omgeving, of door ouderdom. MTB staat erom bekend dat het tientallen jaren kan overleven in een granuloom, om daarna weer actief worden. Omdat granulomen niet in staat zijn om MTB-bacteriën te doden, vormen ze dus een soort tikkende tijdbom. In 2018 schatte de Wereldgezondheidsorganisatie dat een kwart van de wereldbevolking geïnfecteerd was met een slapende (of actieve) vorm van MTB! [2]
Granulomen worden door het hele lichaam getransporteerd omdat het immuunsysteem ervan uitgaat dat ze onschadelijk zijn. Als ze openbreken en de ‘slapende’ MTB weer op vrije voeten komt, kan dus elk orgaan aangetast raken. Zo zijn er gevallen bekend van tuberculose in ruggenmerg, oog, genitaliën en alle andere organen die je kunt bedenken. Gelukkig is de enige besmettelijke variant via de longen. Die variant is zó besmettelijk dat de meeste ontwikkelingslanden specifieke programma’s hebben om uitbraken van tuberculose in te dammen [2]. Ondanks deze programma’s blijven voornamelijk landen met beperkte middelen en infrastructuur broedplekken voor tuberculose, en in toenemende mate ook antibioticum-resistente MBT stammen. De Wereldgezondheidsorganisatie onderneemt actie door internationale samenwerkingen op te zetten voor het uitroeien van tuberculose. Met (dure) middelen om tuberculose te detecteren en de verspreiding te volgen kunnen plaatselijke doktoren en wetenschappers veel effectiever uitbraken opsporen. Ook wordt er veel onderzoek gedaan naar de detectie van slapende MTB-infecties in granulomen. Met deze nieuwe methoden hoopt de Wereldgezondheidsorganisatie deze oeroude epidemie in 2035 uit de wereld te helpen [2].
Link to the original post: Zhai, W., Wu, F., Zhang, Y., Fu, Y., Liu, Z. (2019, January 15). The immune escape mechanisms of Mycobacterium tuberculosis. MDPI. https://www.mdpi.com/1422-0067/20/2/340.
Additional sources
- World Health Organization. Global tuberculosis Report. https://www.who.int/teams/global-tuberculosis-programme/tb-reports.
- Gengenbacher, M., & Kaufmann, S. H. E. (2012, May 1). Mycobacterium tuberculosis: Success through dormancy. OUP Academic. https://academic.oup.com/femsre/article/36/3/514/634506.
Featured image: https://www.flickr.com/photos/niaid/5149398656
Vertaald door: Steven Pilon