Microbiologie in hapklare porties
Bitterzoete resistentie
Een bacterieel sprookje
Er was eens een tijd dat bacteriën bang waren voor antibiotica. Niet lang daarna wapenden ze zich met mutaties. Door deze mutaties waren sommige bacteriën in staat om de antibiotica te overwinnen. Het leven was gemakkelijk voor bacteriën! Tot vandaag…
Onderzoekers dachten dat het mechanisme achter antibioticaresistentie eenvoudig was: zodra de bacteriën mutaties tegen een antibioticum hadden verworven, konden ze de levensbedreigende effecten ervan weerstaan. De onderzoekers bedachten verschillende methoden om dit probleem tegen te gaan. L. Galera Laporta en J. Garcia Ojalvo hebben echter ontdekt dat antibioticaresistentie misschien niet zo’n eenvoudig mechanisme is als velen denken. Bacteriën kunnen hun gevoeligheid voor antibiotica veranderen door interactie met hun naburige bacteriën. Daarom zijn de huidige maatregelen tegen antibioticaresistentie misschien niet zo doeltreffend.
Antibioticaresistentie: dynamisch of klassiek?
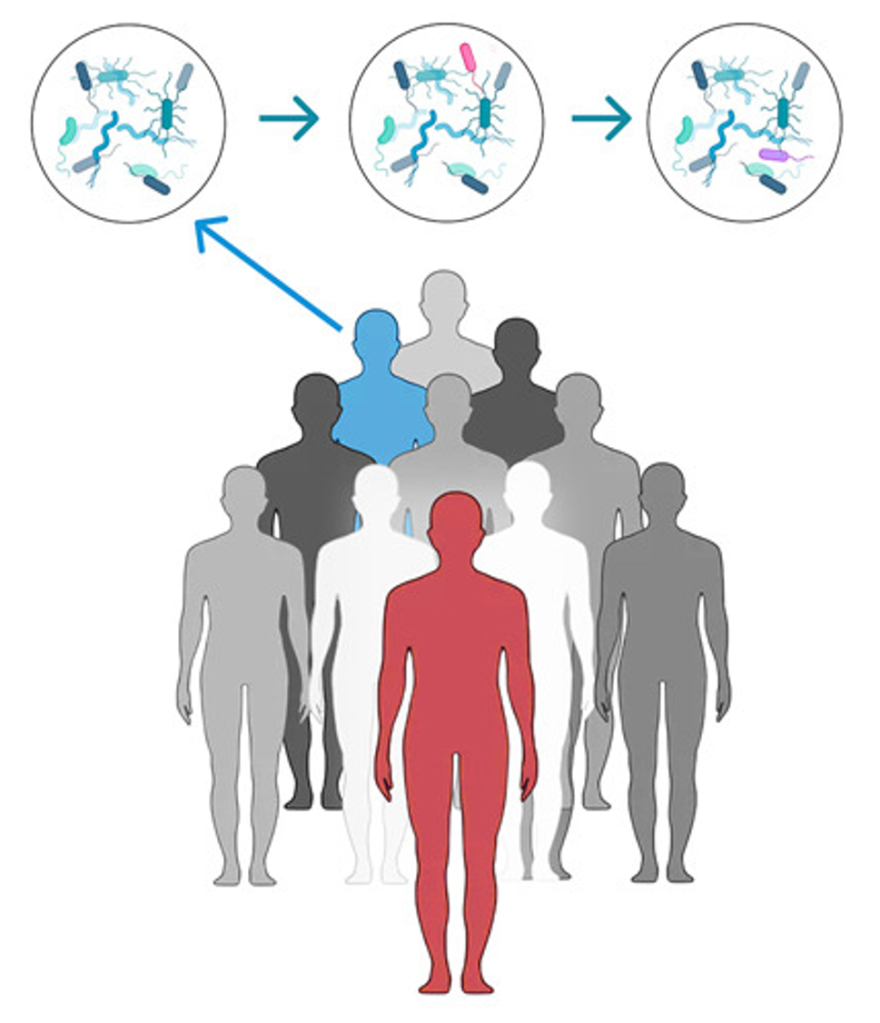
Sommige bacteriën zijn tolerant voor een bepaald type antibioticum, andere voor een ander type. Wanneer twee bacteriën met een verschillende tolerantiegraad voor antibiotica in aanwezigheid van antibiotica worden gegroeid, zijn er vier mogelijke scenario’s (figuur 1): (a) de tolerante bacterie overleeft, de gevoelige bacterie sterft; (b) beide bacteriën kunnen overleven omdat de tolerante bacterie voldoende neutraliserende stofjes aanmaakt om de gevoelige bacterie te helpen het antibioticum te bestrijden; (c) beide bacteriën sterven; (d) de tolerante bacterie sterft ende gevoelige bacterie overleeft, door te profiteren van het vermogen van de tolerante bacterie om neutraliserende stoffen aan te maken.

Ampicilline is een breedspectrum-antibioticum, wat betekent dat het werkzaam is tegen een breed scala van bacteriën. Onderzoekers kozen twee bacteriën met verschillende gevoeligheid voor ampicilline: Bacillus subtilis (B. subtilis) en Escherichia coli (E. coli). Wanneer B. subtilis samen met ampicilline wordt gekweekt, is het tolerant en groeit het, al is het wat langzaam. E. coli is gevoelig en vertoont geen optimale groei. Onderzoekers ontdekten dat wanneer de twee bacteriën samen worden gekweekt, B. subtilis zijn tolerantie voor ampicilline verliest, terwijl E. coli tolerant wordt voor ampicilline en het overleeft. Het lot van de co-cultuur volgde dus de laatste van de vier scenario’s die in de vorige paragraaf zijn uitgelegd.
Het publiek zal zich nu afvragen: “De hele hype over antibioticaresistentie draait om de mutaties die bacteriën tijdens de evolutie hebben verworven. Hoe kwamen de onderzoekers tot deze conclusie van dynamische antibioticaresistentie?” De onderzoekers maakten afzonderlijke culturen van B. subtilis en E. coli met ampicilline, en ook co-culturen. Ze filterden de bacterien van het groeimedium (dat heet supernatant) en kweekten verse culturen van B. subtilis in het supernatant. Ze stelden vast dat B. subtilis het best groeide in supernatant van afzonderlijke culturen van B. subtilis, het slechtst in supernatant van co-culturen van B. subtilis en E. coli, en het slechtst in supernatant van een afzonderlijke cultuur van E. coli (figuur 2).

Hoe kan deze nieuwe informatie de geneeskunde beïnvloeden?
Deze dynamische interactie tussen microben kan worden samengevat als een cooperator-cheater dynamiek. De coöperator is B. subtilis omdat hij het antibioticum neutraliseert. De valsspeler is E. coli omdat deze niets bijdraagt tot het inactiveren van het antibioticum en in plaats daarvan profiteert van al het harde werk van B. subtilis. Laporta en Ojalvo vermeldden in een interview dat deze informatie kan worden gebruikt om de antibioticaresistentie van pathogene bacteriën te beïnvloeden door probiotica te verstrekken die niet-pathogene valsspeelbacteriën bevatten. De aanwezigheid van probiotische bacteriën zal de ziekteverwekker gevoelig maken voor antibiotica, waardoor hij verzwakt.
Betekent dit dat de artsen hun manier van antibiotica voorschrijven moeten veranderen? Lastige vraag! Misschien moeten we nog een paar jaar onderzoek afwachten om daar achter te komen.

Link to the original post: L. Galera-Laporta and J. Garcia-Ojalvo, Antithetic population response to antibiotics in a polybacterial community, Science Advances, 6 march 2020
Distributed under a Creative Commons Attribution NonCommercial License 4.0 (CC BY-NC)
Featured image: Image created by the author
Other references:
1. Özkaya Ö, Xavier KB, Dionisio F, Balbontín R. Maintenance of Microbial Cooperation Mediated by Public Goods in Single- and Multiple-Trait Scenarios. J Bacteriol. 2017 Nov 15;199(22):e00297-17. https://doi.org/10.1128/JB.00297-17
2. Katrina Krämer. Cheating bacterium becomes antibiotic-tolerant at expense of other species. Chemistry World 2020 March 10. https://www.chemistryworld.com/news/cheating-bacterium-becomes-antibiotic-tolerant-at-expense-of-other-species/4011320.article
Vertaald door: Charlotte van de Velde