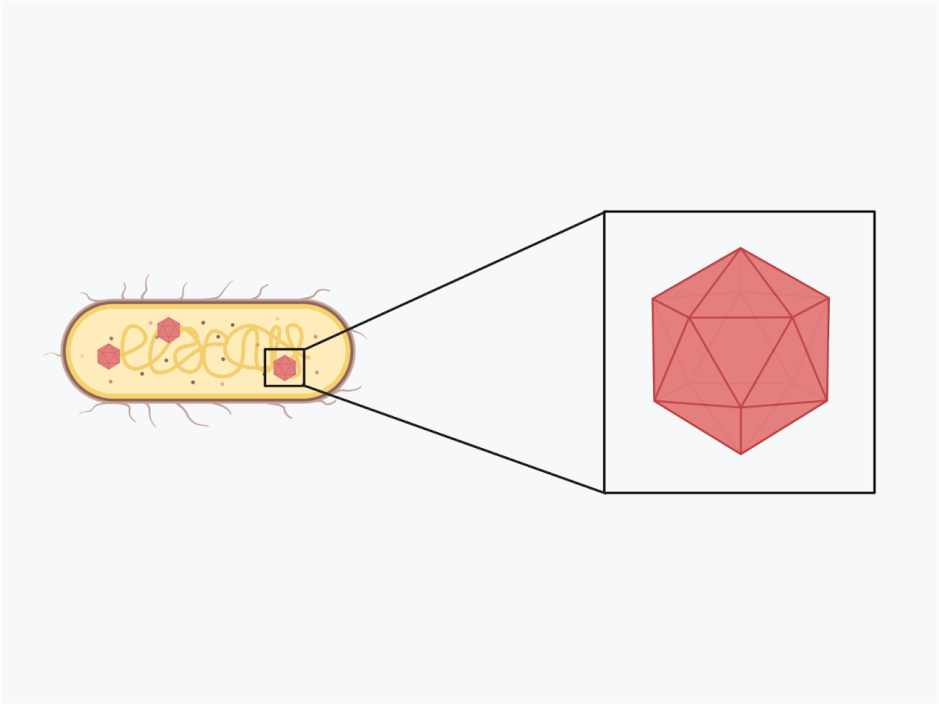
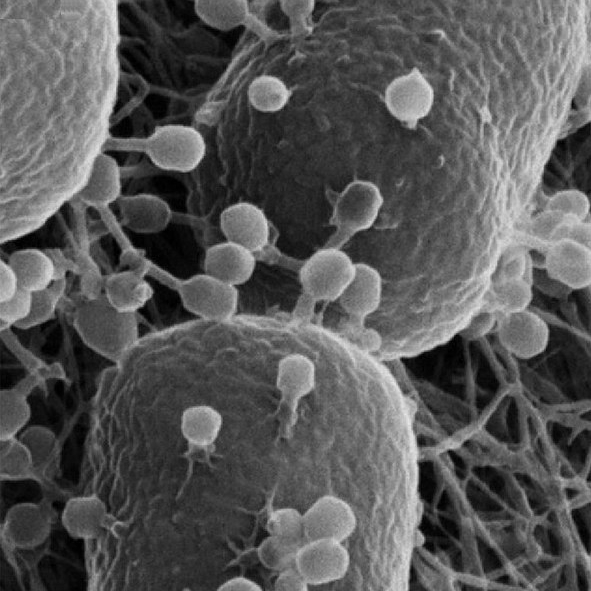
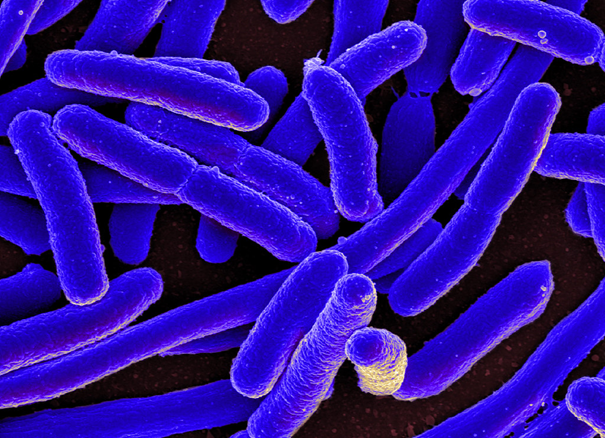
Разбираем мир микробиологии по кусочкам
Оказывается, что ваши кишечные бактерии – это маленькие склады для медицинских препаратов
Вы, наверняка, уже знаете, что терапевтические препараты могут оказывать негативное влияние на микробиом кишечника. Но знаете ли вы, что наш кишечный микробиом может повлиять как на доступность, так и на эффективность терапевтических препаратов? Оказывается, что взаимодействие между бактериями и лекарствами можно описать как улицу с двусторонним движением. Основным механизмом, с помощью которого бактерии влияют на доступность лекарств, является биотрансформация – химическое преобразование лекарств микроорганизмами. Исследование проведенное в 2019 году показало, что более сотни молекул разных препаратов проходят химические преобразования нашими кишечными бактериями. Биотрансформация не всегда имеет один и тот же результат, и полученные вариации зависят как от бактерий, так и от самого препарата. Например, ловастатин и сульфасалазин трансформируются бактериями в свои активные формы, а дигоксин, наоборот, становится менее активным. Несмотря на доказательства связи между эффективностью лекарств и микробной активностью, систематическое изучение этих взаимодействий началось сравнительно недавно.
Биоаккумуляция и кишечные бактерии
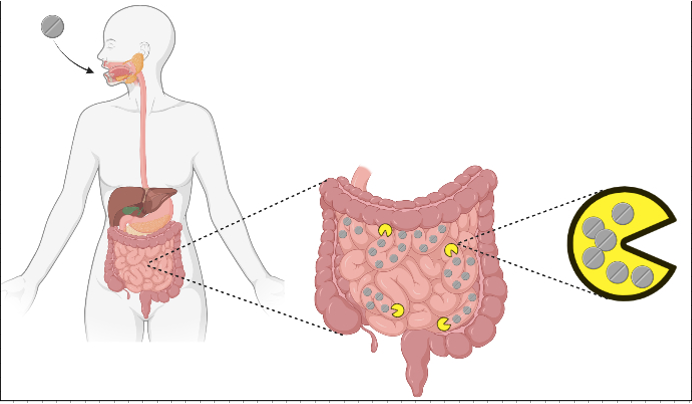
Стремясь расширить наши познания в этой теме, исследователь Klümann с коллегами проанализировали взаимодействия между 15 препаратами и 25 штаммами кишечных бактерий человека (Изображение 1).
Изображение 1: Схематическое изображение экспериментальной установки для изучения взаимодействий бактерий с лекарствами. Источник: оригинальная статья и Biorender.com
Из полученных 375 пар бактерий-лекарств было выявлено 70 взаимодействий, 29 из которых не были ранее зарегистрированы (Изображение 2). Интересно, что 17 из этих новых идентифицированных взаимодействий были результатами не биотрансформации, а биоаккумуляции (накопления препарата бактериями без его модификации). Вдобавок, исследование показало, что эффекты биотрансформации и биоаккумуляции не исключают друг друга.
Изображение 2: Сеть взаимодействий бактерий с лекарствами, которая была установлена в ходе исследования. Слева: процессы биотрансформации или биоаккумуляции лекарств кишечными бактериями. Справа: влияние лекарств на рост кишечных бактерий. Источник: оригинальная статья.
Если механизм биотрансформации лекарств еще возможно представить (полагаясь на изучение метаболических ферментов), то какой механизм лежит в основе биоаккумуляции? Чтобы исследовать молекулярный механизм накопления лекарств, исследователи изучили белки, вступающие в реакцию с дулоксетином в различных штаммах кишечных бактерий, способные к биоаккумуляции. Используя такие методы, как клик-химия и термическое профилирование протеома, они обнаружили несколько белков, которые реагировали с дулоксетином. В дополнение к найденным белкам, исследователи также показали, что соединение дулоксетина с бактериальными метаболическими ферментами изменяет метаболизм штаммов, склонных к биоаккумулиции (Изображение 3). Таким образом, биоаккумуляция не только влияет на доступность лекарства, но и изменяет клеточную физиологию бактерий!
Изображение 3: Слева: схематическое изображение изменения метаболизма в результате биоаккумуляции. Низкомолекулярный препарат, такой как дулоксетин, создает связь с бактериальным “белком-мишенью”, что влияет на его функцию. Справа: путь биосинтеза нуклеотидов у биоаккумулирующей бактерии C.saccharolyticum. Источник: оригинальная статья и Biorender.com
Последствия биоакумуляции препаратов
Метаболические взаимодействия играют фундаментальную роль в формировании состава микробных сообществ кишечника. Тогда возникает вопрос: влияют ли метаболические изменения, связанные с биоаккумуляцией, на состав сообщества? Для поиска ответа, команда исследователей собрала микробные сообщества, состоящие из пяти видов кишечных бактерий, включая и те, что способны к биоаккумуляции дулоксетина (Streptococcus salivarius), и те виды, чей рост останавливается в присутствии дулоксетина (Eubacterium rectale). Они обнаружили, что присутствие дулоксетина заметно изменило состав микробного сообщества, что привело к стократному увеличению численности E.rectale (Изображение 4). Хотя биоаккумуляция дулоксетина у S.salivarius смогла защитить E. rectal от действия препарата, увеличение числа бактерий в присутствии препарата доказало присутствие взаимодействий, стимулирующих рост. Исследователи показали, что аккумуляция дулоксетина бактериями S.salivarius стимулировала рост E.rectal (Изображение 5). Таким образом, лекарственные средства могут изменять микробные сообщества кишечника либо с помощью остановки активности определенных членов микробного сообщества, либо путем модификации метаболических взаимодействий между бактериями одного сообщества.
Изображение 4: Биоаккумуляция дулоксетина изменяет состав микробного сообщества. Источник: оригинальная статья.
Изображение 5: Способная к биоаккумуляции дулоксетина бактерия S.salivarius способствует более активному росту E.rectale. Источник: оригинальная статья и Biorender.com
Наконец, ученые ответили на последний вопрос: как биоаккумуляция влияет на биологический ответ человеческого организма на лекарство? Чтобы это исследовать, Klümann с коллегами изучили реакцию C. elegans на биоаккумуляцию дулоксетина. Поскольку дулоксетин регулирует движение мышц, ученые использовали модель движения животных для эксперимента. Результаты показали, что бактерии, способные к биоаккумуляции дулоксетина, влияют на организм, ослабляя эффект препарата (Дулоксетин замедляет движение/мышечное сокращение. Следовательно, биоаккумуляция дулоксетина снижает доступность этого препарата для человеческих клеток, что приводит к ослабленному терапевтическому эффекту).
В итоге, ученые обнаружили два способа, которые используются кишечными бактериями для биоаккумуляции препарата. Измененная секреция метаболитов может привести к изменениям состава микробного сообщества, что может потенциально повлиять на механизм действия некоторых лекарств. Таким образом, изучение и систематическая запись взаимодействий между лекарствами и бактериями может помочь нам лучше прогнозировать поведение препаратов внутри организма и их влияние на метаболизм бактерий. Такие исследования могут открыть новые горизонты в изучениях состава микробиоты, фармакокинетики, а также побочных эффектов и реакций человека на определенное лекарство.
Перевод был сделан Марией Мартыновой
Link to the original post:
Image created by author with BioRender.com