Deconstruyendo la microbiología mordisco a mordisco
No hay tal cosa como la ineficiencia.
El nitrógeno es el componente principal de toda la vida, siendo este esencial para proteínas y ADN, por ejemplo. A pesar de su abundancia en la tierra, el suministro de nitrógeno es un factor limitante del crecimiento para la mayoría de las formas de vida. No me refiero a los entusiastas del fitness que toman batidos de proteínas para aumentar la masa muscular, sino, por supuesto, a los microorganismos. Las bacterias y las arqueas son las únicas formas de vida capaces de fijar nitrógeno del aire al interior de las células. Eso significa que todo el nitrógeno en nuestro cuerpo (pero también en el de otros animales o plantas) ha sido “preparado” para nosotros por bacterias y arqueas. Las únicas enzimas que se sabe que catalizan este proceso se denominan nitrogenasas.
Existen tres variantes de estas nitrogenasas, que llevan el nombre de diferentes metales que se encuentran en su sitio activo: molibdeno (Mo), vanadio (V) y hierro (Fe). Las enzimas toman nitrógeno de la atmósfera y alguna fuente de electrones para reducir el N2 a NH3, pero también producen una variedad de subproductos (principalmente H2). De las tres variantes, la Mo-nitrogenasa es la enzima más antigua y las otras dos evolucionaron a partir de ella (1). Sin embargo, la Mo-nitrogenasa también se considera la enzima de fijación de nitrógeno más eficiente porque produce la menor cantidad de subproductos (1). Entonces, si la V- y la Fe-nitrogenasa son menos eficientes en su trabajo, ¿por qué habrían evolucionado?
Katja Luxem y sus colegas de la Universidad de Princeton, Nueva Jersey, se propusieron encontrar respuestas utilizando Rhodopseudomonas palustris (2). Esta bacteria contiene los genes de las tres enzimas, pero, como muestra el artículo, generalmente depende de la Mo-nitrogenasa para su suministro de nitrógeno. Además, los investigadores probaron tres mutantes genéticas de R. palustris, cada uno de los cuales contenía solo una de las isoenzimas nitrogenasas. Descubrieron que, dependiendo de la fuente de carbono, la Mo-nitrogenasa no fijaba el nitrógeno más rápido. La V-nitrogenasa soportó un crecimiento más rápido en otros sustratos, y en acetato incluso superó al la wild-type (Figura 1).
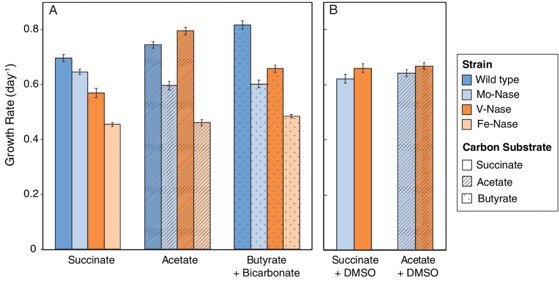
Cuando se la alimenta con acetato, la mutante que expresa solo V-nitrogenasa produce tanto subproducto (H2) como la wild-type. Los autores sospechan que tiene que ver con la temperatura: la idea de que la Mo-nitrogenasa es la más eficiente surgió de experimentos a 30 °C, pero este experimento se llevó a cabo a 19 °C, y no son los primeros en ver caer la eficiencia de la nitrogenasa de Mo a temperaturas más bajas (3). Por lo tanto, la existencia de la V-nitrogenasa junto a la Mo-nitrogenasa podría tener que ver con la temperatura del entorno en el que vive la bacteria.
Luxem y sus colegas también muestran que la eficiencia de la fijación de nitrógeno no depende únicamente de las nitrogenasas, sino de toda una cascada de enzimas y cofactores que entregan los electrones y la energía para la catálisis. Usando proteómica, encontraron que la mutante V-nitrogenasa, que se desempeñaba tan bien con acetato, estaba respaldada por un sistema de proteínas de suministro de energía muy similar al tipo wild-type. El mutante que portaba sólo la Mo-nitrogenasa tenía un perfil diferente de enzimas de soporte. Por lo tanto, la evolución de diferentes formas de nitrogenasa también podría estar relacionada con la interacción con otras proteínas.

Curiosamente, R. palustris no compensa las nitrogenasas más lentas gastando más recursos en la fijación de nitrógeno. Además del nitrógeno, R. palustris también puede fijar carbono a partir de CO2 (en un proceso similar a la fotosíntesis). Para fijar cualquiera de los elementos, se requieren electrones. Por lo tanto, la bacteria debe equilibrar la cantidad de cada una que fija (consulte la Figura 2, flechas E y F). En los experimentos de Luxem, el suministro de nitrógeno es limitante para el crecimiento de R. palustris (y se le da toda la fuente de carbono que podría necesitar). Por tanto, parecería útil redirigir tantos electrones como sea posible a la fijación de nitrógeno. Sin embargo, los autores informan algo diferente: el porcentaje de electrones disponibles utilizados para la reducción de N se mantiene constante, alrededor del 60%, para diferentes fuentes de carbono y enzimas nitrogenasas. Esto es especialmente sorprendente para la Fe-nitrogenasa, que fija muy poco N2 a expensas de producir una gran cantidad de H2. Los autores proponen que existe cierta presión de selección evolutiva (aún desconocida) contra la abolición de la fijación de carbono.
En resumen, parece que la V-nitrogenasa “inútil” simplemente nunca se examinó de una manera que mostrara su fuerza: la fijación de nitrógeno a temperaturas más bajas. Gracias a Luxem y su equipo, hemos podido vislumbrar en qué es buena. ¡Y a su debido tiempo, sin duda, también apreciaremos las ventajas de la Fe-nitrogenasa!
Link to the original post: Carbon substrate re-orders relative growth of a bacterium using Mo-, V-, or Fe-nitrogenase for nitrogen fixation Katja E. Luxem, Anne M. L. Kraepiel, Lichun Zhang, Jacob R. Waldbauer, Xinning Zhang
Imagen publicada: https://commons.wikimedia.org/wiki/File:Nitrogen_Cycle_1.svg
Escrito por Steven Pilon
Traducido por: Santiago Chaillou