Microbiologie in hapklare porties
Inefficiëntie bestaat niet.
Stikstof is een hoofdingrediënt voor al het leven, bijvoorbeeld vanwege zijn onmisbare positie in eiwitten en DNA. Hoewel het element vrij veel voorkomt op aarde, is de beschikbaarheid ervan toch limiterend voor de meeste organismen. Sportschool-types met eiwitshakes hebben daar geen last van, maar bacteriën des te meer. Bacteriën (en archaea) zijn de enige levensvormen die stikstof uit de lucht (N2) in eiwitten, DNA en andere celonderdelen kunnen fixeren. Dat betekent dat de stikstof die in ons zit (maar ook in dieren en planten) ooit is “voorbereid” door een micro-organisme. De enzymen die ze daarvoor gebruiken heten nitrogenasen.
Er bestaan drie soorten nitrogenasen, die zich onder andere onderscheiden door verschillende metalen in het actieve centrum: molybdeen (Mo), vanadium (V) en ijzer (Fe). Ze katalyseren dezelfde reductie van N2 uit de lucht naar NH3, maar produceren ook allerlei bijproducten (hoofdzakelijk H2). Van de drie varianten is de Mo-nitrogenase de oudste, en de andere twee zijn later uit de Mo-nitrogenase geëvolueerd (1). Mo-nitrogenase staat ook als de meest efficiënte van de drie te boek, omdat het de minste bijproducten levert (1). Als dus de V-nitrogenase en Fe-nitrogenase minder goed zijn in hun taak, wat heeft dan hun evolutie aangedreven?
Katja Luxem en haar collega’s aan de universiteit van Princeton (VS) wilden deze vraag beantwoorden met hun model-organisme Rhodospeudomonas palustris. Deze bacterie bevat de genen voor alledrie de nitrogenasen, maar – zoals het artikel laat zien – is onder standaard-omstandigheden afhankelijk van Mo-nitrogenase voor de toevoer van gebonden stikstof. Naast de “gewone” bacterie, onderzocht het team ook drie genetische mutanten ervan die slechts één van de nitrogenasen bevatte. Uit hun onderzoek blijkt dat de koolstofbron in het groeimedium bepaalt welke nitrogenase het beste werkt. Zo ondersteunde V-nitrogenase de snelste groei op acetaat en butyraat, en niet de Mo-nitrogenase (Figuur 1).
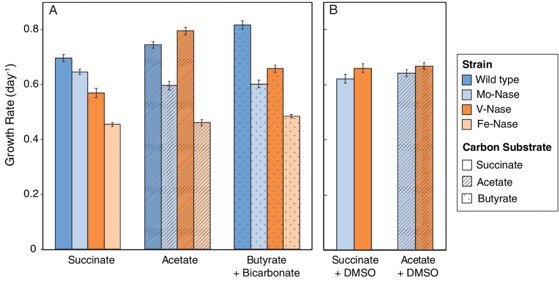
De mutant met alleen V-nitrogenase produceerde in de voedingsbodem met acetaat dezelfde hoeveelheid bijproduct (H2) als het wild-type. De auteurs vermoeden dat dit te maken heeft met temperatuur: het klassieke beeld van Mo-nitrogenase als efficiëntste enzym komt van de “standaard-omstandigheden” bij 30 °C, terwijl dit experiment bij 19 °C plaatsvond. Het is ook niet de eerste keer dat Mo-nitrogenase bij lagere temperaturen slecht uit de test kwam (3). Het bestaansrecht van V-nitrogenase kan dus, behalve met koolstofbron, ook met wisselende buitentemperatuur te maken hebben.
Luxem en haar collega’s laten ook zien dat de snelheid van stikstof-fixatie wordt beïnvloed door allerlei eiwitten die de nitrogenasen in hun functie ondersteunen. Er moeten bijvoorbeeld gebonden elektronen richting de nitrogenase getransporteerd worden om de katalyse te kunnen laten verlopen. Met proteomica bewezen de auteurs dat de V-nitrogenase mutant, die op acetaat zo snel kon groeien, een vergelijkbare ondersteuning voor de nitrogenase had als in de wild-type. De mutant die alléén Mo-nitrogenase bevatte bleek een andere verdeling van ondersteundende eiwitten te hebben. De evolutie van meerdere vormen van nitrogenase zou dus ook verbonden kunnen zijn aan de interactie met samenwerkende eiwitten.

Voor ‘slomere’ nitrogenasen compenseert R. palustris kennelijk niet door meer grondstoffen aan stikstoffixatie te wijden. R. palustris kan namelijk naast stikstof, ook koolstof fixeren (in een fotosynthese-achtig proces). Voor zowel stikstof- als koolstoffixatie zijn elektronen nodig, dus moet de cel een balans vinden hoeveel grondstof er naar elk proces gaat. Omdat koolstof voor de cel ruim voorhanden is én stikstof groei-limiterend onder deze laboratorium-omstandigheden, zou het logisch lijken om de elektronen helemaal in de stikstof-fixatie te steken. De auteurs vonden echter dat per percentage van elektronen voor stikstof-fixatie constant bleef rond 60%, ongeacht de nitrogenase-mutant of koolstofbron. Dit is met name opvallend voor de Fe-nitrogenase, die relatief weinig N2 weet te reduceren ten koste van veel H2-productie. Het artikel suggereert dat er een (nog onbekende) selectiedruk in de natuur bestaat om koolstof-fixatie te verminderen.
Zo blijkt dat de “nutteloze” V-nitrogenase nog nooit onder de juiste omstandigheden was onderzocht om zijn sterke kant te laten zien. Dankzij Katja Luxem en haar collega’s weten we nu dat verschillende koolstofbronnen en temperatuurverschillen het beste in dit enzym naar boven kunnen halen. Het is een kwestie van tijd voordat we de kracht van Fe-nitrogenase ook zullen leren waarderen!
Link to the original post: Carbon substrate re-orders relative growth of a bacterium using Mo-, V-, or Fe-nitrogenase for nitrogen fixation Katja E. Luxem, Anne M. L. Kraepiel, Lichun Zhang, Jacob R. Waldbauer, Xinning Zhang
Featured image: https://commons.wikimedia.org/wiki/File:Nitrogen_Cycle_1.svg
Vertaald door: Steven Pilon