Deconstruyendo la microbiología mordisco a mordisco
AUna antigua arma química contra los depredadores virales.
Los virus no pueden diseminar su material genético por sí mismos. Para su proliferación es crucial la capacidad de infectar un organismo hospedador y cooptar los recursos del hospedador para la transcripción y replicación viral. Muchos fármacos antivirales potentes utilizados para el tratamiento clínico de virus humanos, como el herpes, el VIH, o la hepatitis C, se dirigen a las funciones de transcripción y replicación viral. Específicamente, estas terapias son moléculas pequeñas que funcionan como imitaciones de nucleótidos, los bloques de construcción de ARN y ADN, que son incorporados por polimerasas virales durante la síntesis de ARN o ADN. Los imitadores son como eslabones de cadena rotos, ya que su incorporación evita la adición de más nucleótidos por las polimerasas virales, terminando así la polimerización. La consecuencia de esto es la inhibición de la replicación viral. De hecho, esta estrategia clínica es análoga a una estrategia antiviral ya presente en la naturaleza.
Durante la infección viral, los seres humanos producen moléculas que terminan la cadena de nucleótidos, y esta capacidad se basa en una proteína llamada viperina. La viperina cataliza la conversión del ribonucleótido CTP (un componente del ARN) en una molécula modificada llamada ddhCTP. Al igual que los imitadores clínicos de moléculas pequeñas, el ddhCTP inhibe la transcripción y replicación viral, lo que permite una amplia actividad antiviral contra los virus de ARN y ADN.
Al igual que los humanos, los procariotas, que incluyen bacterias y arqueas, deben defenderse de los depredadores virales. El “sistema inmunológico” de los procariotas en comparación con el sistema inmunológico humano es muy diferente. Sorprendentemente, sin embargo, Bernheim y sus colegas descubrieron recientemente que la capacidad humana para sintetizar terminadores de cadenas de nucleótidos probablemente se originó en procariotas. Su trabajo se inspiró en la observación de que algunas bacterias y arqueas (alrededor del 1%) codifican homólogos de la viperina humana. Aquí, los investigadores demostraron por primera vez que las supuestas viperinas procariotas, o pVips, se defienden de los virus que infectan bacterias llamados fagos, mediante la producción de nucleótidos que terminan la cadena.
Dado su descubrimiento de que algunos procariotas codifican homólogos de viperina, los investigadores plantearon la hipótesis de que estas proteínas, como la viperina humana, podrían funcionar como defensa antiviral. Para probar esto, los investigadores expresaron pVips en el organismo modelo bacteriano Escherichia coli y desafiaron a E. coli con una variedad diversa de fagos. Descubrieron que los pVips podían proteger o reducir la infección. La actividad enzimática del pVip fue fundamental para esta protección, ya que la mutación de las características clave requeridas para la catálisis anuló la capacidad de defensa contra los fagos. Sorprendentemente, en otra repetición de este experimento, las E. coli que expresaban el gen de la viperina humana también estaban protegidas contra la infección por fagos. Por tanto, una proteína humana puede combatir un virus específico de una bacteria. Juntos, sus hallazgos sugirieron que la función de los pVips procarióticos era similar a la de la viperina humana y, además, que el mecanismo de defensa está altamente conservado entre los organismos filogenéticamente distantes.
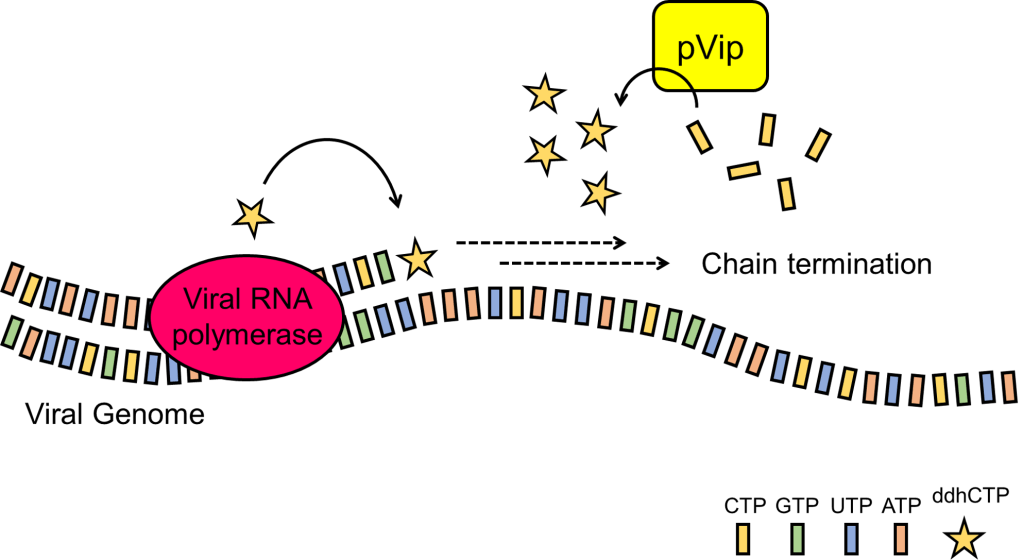
La síntesis de ddhCTP es clave para la función antiviral de la viperina humana. Por lo tanto, el siguiente objetivo de los investigadores fue demostrar que los pVips procarióticos también producen esta arma química. El análisis de las moléculas pequeñas recogidas de E. coli que expresan pVips reveló la presencia de ribonucleótidos ddhCTP. Además, algunos pVips podrían sintetizar otras moléculas de terminación de cadena como ddhUTP o ddhGTP (derivados de los ribonucleótidos de ARN UTP y GTP, respectivamente). Select pVips también tenía la capacidad de producir múltiples nucleótidos de terminación de cadena, lo que sugiere que estos pVips son promiscuos y podrían albergar un arsenal diverso para proteger contra la infección por fagos. Además, demostraron que, en un tubo de ensayo, las proteínas pVip purificadas convertían los ribonucleótidos en sus versiones modificadas. Por lo tanto, la producción de terminadores de cadena como ddhCTP, ddhGTP y ddhUTP es clave para la función antiviral de pVip.
Finalmente, para comprender los orígenes evolutivos de pVips, Bernheim y sus colegas agruparon pVips en grupos basándose en la similitud de la secuencia de ADN. Curiosamente, su análisis reveló que las viperinas humanas no eran las más divergentes de las pVips codificadas por bacterias y arqueas. Más bien, las viperinas humanas se colocan entre un grupo dominado por especies de arqueas y un grupo compuesto por bacteroides, un filo específico de bacterias, siendo los parientes más cercanos de las viperinas humanas los pVips de las arqueas. Este hallazgo sugirió que los eucariotas (la delineación de la que los humanos son parte) probablemente adquirieron las viperinas de las arqueas en lugar de desarrollar pVips de forma independiente.
Las bacterias despliegan una diversidad de estrategias para combatir los fagos depredadores. El conocimiento de las estrategias de defensa bacteriana ha proporcionado una gran cantidad de herramientas moleculares para los científicos. Por ejemplo, las proteínas llamadas endonucleasas de restricción, que las bacterias utilizan para cortar material genético viral invasor, son ampliamente utilizadas por los biólogos moleculares para diseñar ADN. Las estrategias de defensa bacteriana también podrían ser información útil para los enfoques clínicos para tratar la infección viral en humanos. Curiosamente, las estrategias de defensa química de moléculas pequeñas no se observan ampliamente en procariotas; pVips es uno de los pocos ejemplos reportados. Quizás los microbios antiguos albergan una gran cantidad de pequeñas moléculas antivirales que podrían aplicarse en un entorno clínico. Estas, sin embargo, aún esperan ser descubiertas.
Link to the original post: Bernheim A., Millman A., Ofir G., Meitav G., et al. Prokaryotic viperins produce diverse antiviral molecules. Nature. 2021. 589(7840): 120-124.
Featured image: Escherichia coli with phages from Wikicommons under the creative commons 4.0 licence
Traducido por: Santiago Chaillou