Microbiologie in hapklare porties
Een oeroud chemisch wapen tegen virussen.
Virussen kunnen hun genetisch materiaal niet zelfstandig verspreiden. Voor hun voortbestaan is het cruciaal om een gastheer te kunnen infecteren, en de middelen van zo’n cel in te gebruiken om virusdeeltjes te vermeerderen. Virale transcriptie- en translatiemechanismen zijn dan ook het doelwit van veel antivirale medicijnen die worden ingezet tegen virussen als herpes, HIV of hepatitis C. Zulke medicijnen lijken op nucleotiden, de bouwstenen van RNA en DNA, zodat ze door virale polymerasen worden ingebouwd tijdens de bouw van viraal DNA of RNA. Zo’n nep-nucleotide fungeert als kapotte schakel in de keten: op de plaatsen waar het wordt ingebouwd, kan de DNA- of RNA-keten niet verder groeien. Dat betekent dus dat de virale transcriptie onderbroken wordt. Deze strategie uit de geneeskunde komt ook in de natuur voor.
Bij een virale infectie produceert de mens stoffen die nucleotide-ketens stopt, met het enzym viperine. Viperine katalyseert de omzetting van CTP (een bouwsteen van RNA) naar het chemisch vergelijkbare ddhCTP. Net zoals de medicijnen blokkeert ddhCTP virale transcriptie en translatie, en biedt daarmee bescherming tegen DNA- en RNA-virussen.
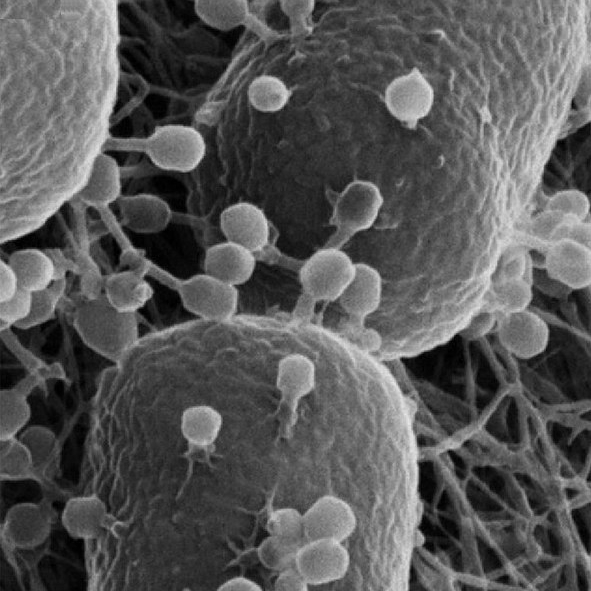
Net als mensen moeten ook bacteriën en archaea zich tegen virussen verdedigen. Het immuunsysteem van prokaryoten verschilt enorm van het menselijke. Als grote verrassing konden Aude Bernheim en haar collega’s aantonen dat de menselijke truc waarschijnlijk zijn oorsprong in prokaryoten vond. De inspiratie voor dit onderzoek kwam na de observatie dat zo’n 1% van alle prokaryoten homologen bevatten van het menselijke viperine (pVip’s). De wetenschappers toonden aan dat de vermoedelijke prokaryote viperines bescherming bieden tegen bacteriofagen (een type virus specifiek voor bacterien) via keten-blokkerende nucleotiden.
De onderzoekers namen de genen van een aantal vermoedelijke pVip’s en brachten die in Escherichia coli tot expressie. Vervolgens infecteerden ze de E. coli-stammen met een brede selectie bacteriofagen, en zagen dat de pVip’s infecties konden verminderen of geheel konden afweren. Genetische mutaties op plekken die waarschijnlijk het actieve centrum uitmaken bleken de functie van de pVip’s weer uit te schakelen – dat wijst erop dat de enzymatische activiteit van pVip’s van belang is voor de bescherming. Daarnaast vond Bernheim dat ook het menselijke viperine in E. coli bescherming biedt tegen bacteriofagen, wat de brede werking van het enzym demonstreert. Zo lijken menselijk viperine en prokaryote pVip’s nauw verwant, en is het beschermingsmechanisme tegen virussen sterk geconserveerd in genetisch onverwante organismen.
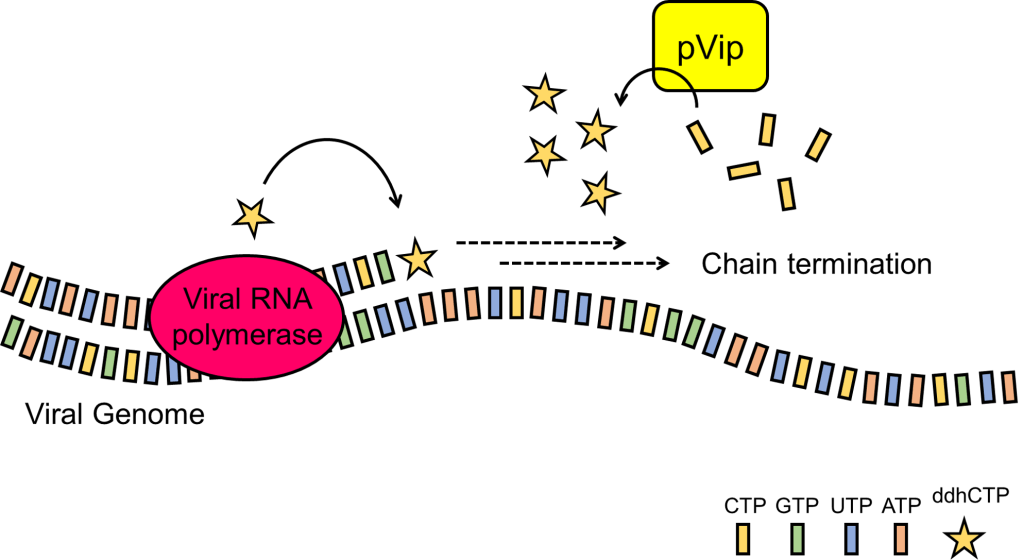
De synthese van ddhCTP is essentieel voor de antivirale werking van menselijk viperine. De wetenschappers zochten uit of ook pVip’s dit chemische wapen produceren. ddhCTP werd inderdaad aangetoond in de E. coli-stammen met pVip-genen met behulp van moleculaire analyse (metabolomics). Ook troffen de onderzoekers pVip’s aan, die ddhUTP of ddhGTP (vanuit de RNA-bouwstenen UTP en GTP) produceerden. Enkele pVip’s maakten zelfs meerdere van deze keten-brekers, wat de cellen een gemengd arsenaal tegen virussen biedt. Deze resultaten uit levende cellen waren ook na te bootsen in een reageerbuisje, met opgezuiverde pVip-enzymen en nucleotiden. De antivirale functie van pVip’s is dus het produceren van keten-brekers zoals ddCTP, ddUTP en ddGTP.
Om de evolutionaire oorsprong van pVip’s te vinden, groepeerden Bernheim en collega’s alle bekende pVip-genen op basis van overeenkomsten in de sequenties. In deze proef bleek menselijk viperine niet veel te verschillen van veel prokayote pVip’s, terwijl sommige pVip’s juist wél ver doorgeëvolueerd zijn. Menselijk viperine zit qua basenparen-volgorde tussen een groep pVip’s uit veelal archaea en een groep met pVip’s uit Bacteroides. Dat doet vermoeden dat de eukaryoten (waar mensen onderdeel van zijn) waarschijnlijk het gen voor viperine hebben gekregen van een prokaryoot, in plaats van dat het gen in eukaryoten is ontwikkeld.
Bacteriën gebruiken een heel scala aan wapens tegen virale predatoren. Kennis over deze afweermechanismen geeft de wetenschapper meer handvaten in het onderzoek. Zo zijn bijvoorbeeld “restrictie-endonucleasen”, enzymen die viraal DNA in bacteriën kapot knippen, nu dagelijkse kost voor experimenten met genetische modificatie. Bacteriële afweermechanismen kunnen ook inspiratie bieden voor klinische behandelingen in mensen. Interessant is dat afweermechanismen met kleine moleculen niet vaak voorkomen in prokaryoten; dit systeem met ddhCTP is een uitzondering. Misschien zijn er nog oeroude microben met antivirale stoffen die als antiviraal medicijn ingezet kunnen worden! Maargoed, dan moeten we ze eerst vinden.
Link to the original post: Bernheim A., Millman A., Ofir G., Meitav G., et al. Prokaryotic viperins produce diverse antiviral molecules. Nature. 2021. 589(7840): 120-124.
Featured image: Escherichia coli with phages from Wikicommons under the creative commons 4.0 licence
Vertaald door: Steven Pilon