Разбираем мир микробиологии по кусочкам
Разрушение патогенов с помощью молекул РНК
В последнее время мы много слышим об РНК в РНК-вакцинах. Но что такое РНК? РНК расшифровывается как РибоНуклеиновая Кислота. Другими словами, это нуклеиновые кислоты, подобные ДНК, но с пятиуглеродной молекулой сахара рибозой. Молекула РНК, которая упоминается все чаще, — это мРНК или матричная РНК. Как следует из названия, это своего рода мессенджер, который передает сообщение от ДНК, копируя его и доставляя на рибосомы, и с помощью тРНК транслируют в белки. В случае с вакцинами, это мессенджер, который сообщает нашим клеткам как сделать шиповидный белок из SARS-CoV-2, чтобы он мог научить иммунную систему распознавать вирус.
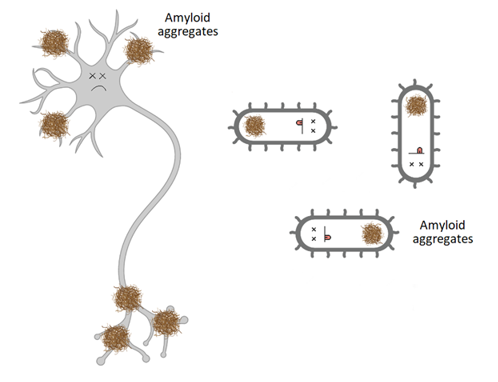
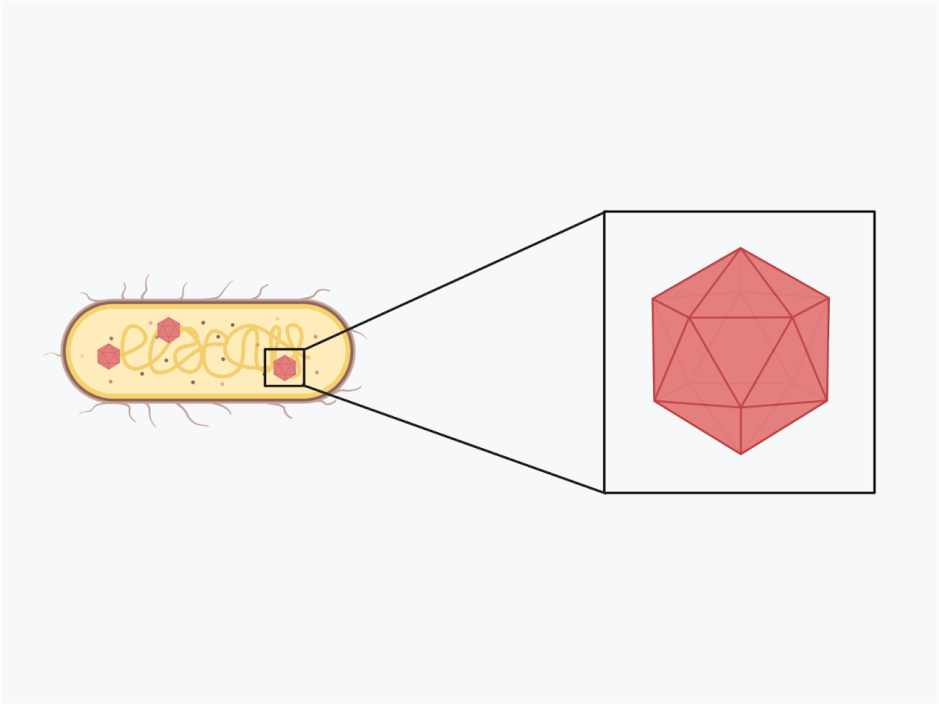
мРНК – не единственные молекулы РНК. Существуют также тРНК (транспортная РНК, обсуждаемая здесь), рРНК (часть строительного блока рибосом), мяРНК (малые ядерные РНК, расположенные в ядре) и другие некодирующие РНК, как малые РНК (мРНК или small RNA – sRNA) (Изображение 1).
Бактериальные sRNAs играют важную роль регуляторных молекул. Обычно они связываются с белками-мишенями и изменяют их функцию, хотя они также могут взаимодействовать с мРНК, которая напрямую регулирует экспрессию генов. Таким образом, они участвуют во многих различных механизмах, связанных с:
- Реакцией на стресс
- Регуляцией транскрипции
- Регуляцией белков наружной мембраны
- Вирулентностью возбудителя болезней
- Чувством кворума (система бактериальной коммуникации)
- Формированием биопленки
- Устойчивостью к антибиотикам
Неудивительно, что эти регуляторные механизмы необходимы для жизнедеятельности патогенных бактерий. Эти бактерии регулируют экспрессию своих генов, чтобы обойти защиту иммунной системы и вызвать заболевание. Использование sRNA для регуляции экспрессии генов является быстрым и эффективным способом по сравнению с более традиционными факторами транскрипции (белками). Многие регуляторные РНК, и особенно у патогенных бактерий, уже изучены, но до сих пор неясно, принимают ли они участие в становлении заболевания.
В своем недавнем исследовании команда разработала генетическую систему для изучения sRNA и их влияния на патогенность бактерий, вызывающих хламидии: Chlamydia trachomatis. Хламидии – это бактерии, поражающие наши клетки и вызывающие различные заболевания. Chlamydia trachomatis является наиболее распространенной причиной бактериальных заболеваний, передающихся половым путем: ежегодно в США регистрируется более 1,8 миллиона новых случаев. Эти бактерии также могут вызывать инфекционную слепоту, называемую трахомой, тогда как родственные виды, такие как C. pneumoniae, вызывают пневмонию.
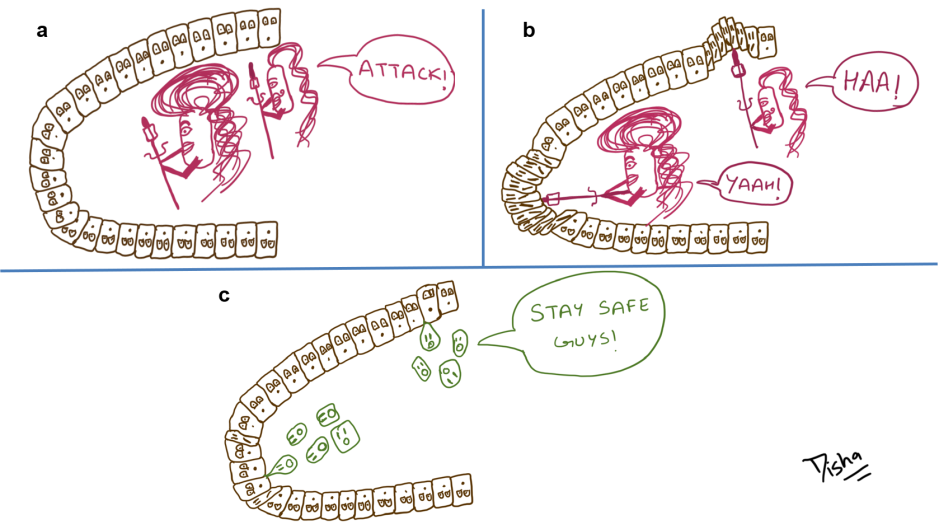
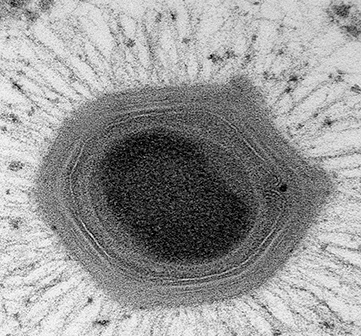
Все бактерии вида Chlamydia имеют одинаковый цикл развития, который чередуется между двумя формами в эукариотической клетке-хозяине. Инфекционная форма, называемая элементарным тельцем (ЭТ синего цвета), связывается с клеткой-хозяином и проникает в нее. Через несколько часов ЭТ дифференцируется в более крупную внутриклеточную форму, известную как сетчатое тельце (СТ выделено красным), в вакуоли, называемой включением. СТ метаболически активны и проходят несколько кругов репликации, прежде чем снова превратиться в ЭТ. Этот шаг имеет решающее значение для передачи заболевания, потому что только ЭТ могут инфицировать новые клетки-хозяева (Изображение 2).
В этом исследовании авторы провели скрининг тринадцати хламидийных sRNA на их воздействие на развитие инфекции, и идентифицировали несколько, сверхэкспрессия которых вызывала серьезное снижение инфекции. В частности, сверхэкспрессия sRNA CtrR3 вызывала дефект конверсии СТ в ЭТ (зеленая sRNA, Изображение 3). Поэтому ЭТ плохо формировались и не могли инфицировать большее количество клеток. Другая сверхэкспрессия sRNA CtrR7 вызывала дефект репликации СТ (синяя sRNA, Изображение 3). На этот раз СТ не могли эффективно реплицироваться, уменьшая количество продуцируемых ЭТ и, тем самым, сдерживали темпы инфекции.
Ученые объединили генетический подход к исследованию с биохимическим, биоинформационным, мутационным и функциональным анализом, чтобы идентифицировать мишень для sRNA. В этом случае мишенями были мРНК, участвующие в важных стадиях развития инфекции. Это исследование имеет важное значение для будущих исследований патогенов и открывает двери для потенциальных областей лечения. В то время как sRNA ранее изучались на модельных организмах, таких как E. coli, крайне важно, чтобы регуляция после транскрипции была изучена и у патогенов, чтобы в будущем разработать методы лечения, которые снизили бы инфекционность патогена или его вирулентность, чтобы сделать лечение более эффективным или непосредственно действовать как антибиотик.
Перевод был сделан Марией Мартыновой
Оригинальная статья: Wang, K., Sheehan, L., Ramirez, C., Densi, A., Rizvi, S., Ekka, R., … Tan, M. (2022). A Reverse Genetic Approach for Studying sRNAs in Chlamydia trachomatis. MBio. https://doi.org/10.1128/mbio.00864-22
Изображение: адаптировано из https://upload.wikimedia.org/wikipedia/commons/d/da/DNA_RNA_structure_%28full%29.png