Mikrobologie in kleinen Häppchen
Wie Bakterien ihre Ernährung umstellen
Antibiotika. Insulin. Vitaminpräparate. Biokraftstoffe. Detergenzien. Was haben diese Dinge gemeinsam? Sie werden alle von Mikroben hergestellt. Die Biotechnologieindustrie nutzt verschiedene Mikroorganismen als winzige Fabriken für die groß angelegte Produktion weit verbreiteter Chemikalien. Der Deal ist relativ einfach: Sie geben uns, was wir wollen, und erhalten dafür ihr Lieblingsessen und eine Umgebung, in der sie sich wohlfühlen. Was aber, wenn ihre Lieblingssnacks auch unsere Lieblingssnacks sind? Könnten wir den Bakterien beibringen, etwas anderes zu mögen? Eine internationale Gruppe von Forschenden hat untersucht, wie ein Bakterium lernt, etwas zu essen, was es nicht gewohnt ist, und wie es seinen Stoffwechsel an diese neue Mahlzeit anpasst.
Mikroben sind Naschkatzen
Mikroben, die in der biotechnologischen Industrie eingesetzt werden, haben eine besondere Vorliebe für Zucker – und wer kann es ihnen verdenken? Der allgemeine Favorit scheint Glukose zu sein, die leicht aus Stärke gewonnen werden kann. Stärke ist im Grunde ein großes Molekül, das aus vielen Glukoseeinheiten besteht, die als lange Kette miteinander verbunden sind. In den meisten Fällen stammt die Stärke aus Produkten wie Mais, Weizen oder Kartoffeln. Doch die Sache hat einen Haken: All diese Lebensmittel essen auch wir Menschen gerne. Könnten wir also die Mikroben mit etwas füttern, das wir Menschen nicht gerne essen?
Wenn ein Maisfeld abgeerntet ist, bleibt eine Menge grüner Biomasse wie Halme und Blätter zurück. Diese enthalten ebenfalls viele Zucker, aber in einer Form, die wir Menschen nicht verdauen können. Wenn Du auf einem Maisblatt herumkaust, wird es am Ende wieder ausgeschieden, ohne Deinem Körper Nährstoffe geliefert zu haben. Und möglicherweise bekommst Du sogar eine Magenverstimmung. Wenn diese für uns unverdaulichen Grünabfälle also zur Fütterung der Mikroben verwendet werden könnten und damit die leckeren Produkte für uns übrigblieben, dann wäre der ganze Prozess billiger und nachhaltiger.
Ernährungsumstellung bei Mikroben
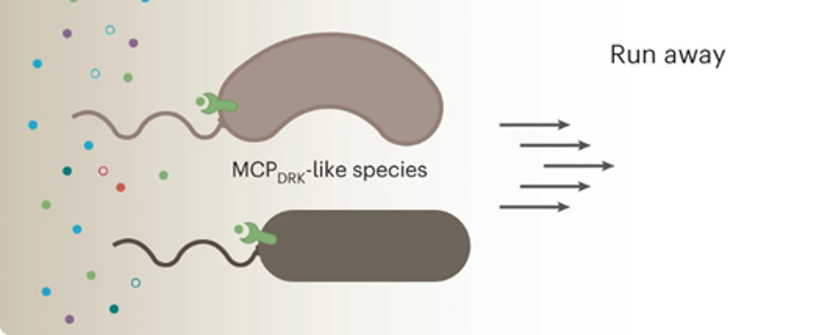
Aber es ist gar nicht so einfach, industrielle Mikroben mit Grünabfällen anstelle ihres Lieblingszuckers zu füttern. Denn dazu muss die Mikrobe ihren Stoffwechsel umprogrammieren, damit sie andere Zucker wie Xylose verdauen kann. Xylose ist ein Bestandteil der Grünabfälle und nach Glukose der zweithäufigste Einfachzucker auf der Erde. Viele Organismen, die in der Biotechnologie eingesetzt werden, können sich nicht von Xylose ernähren. Andere wiederum können Xylose verwerten, ziehen aber Glukose vor. Ein Team der Masaryk-Universität in der Tschechischen Republik hat in Zusammenarbeit mit Forschenden aus Australien, Irland, Deutschland und Spanien untersucht, wie sich das Bakterium Pseudomonas putida, eine der am häufigsten in der Biotechnologie verwendeten Mikroben, an die Ernährung mit Xylose anpasst.
Pseudomonas putida wächst schnell und ist relativ kostengünstig zu züchten, was es zu einer der prominentesten Minifabriken in der Biotechnologiebranche macht. Aufgrund seiner Beliebtheit untersuchen Forschende dieses Bakterium aus allen möglichen Blickwinkeln, um es so gut wie möglich zu verstehen. In einem früheren Beitrag hat maaikeloopt zum Beispiel beschrieben, wie sich dieses Bakterium an herausfordernde Arbeitsbedingungen anpasst. Die Forschenden in unserer Studie wollten herausfinden, wie eine Mikrobe sich an neuartige Mahlzeiten gewöhnt. Da P. putida sich nicht auf natürliche Weise von Xylose ernähren kann, ist dieses Bakterium der perfekte Organismus, um diese Frage zu untersuchen. Zuvor hatte eine andere Gruppe von Forschenden das Bakterium so verändert, dass es Xylose zumindest aufnehmen konnte. Allerdings war dieser Aufnahmeprozess sehr langsam und der genaue Mechanismus wurde nicht untersucht. Die Forschenden unserer Studie wollten daher besser verstehen, was im Inneren des Bakteriums passiert, wenn es seine Ernährung umstellt. Zur Beantwortung dieser Frage nutzten sie die Methode der sogenannten adaptiven Laborevolution (ALE).
Evolution im Reagenzglas
Zunächst veränderten die Forschenden das Bakterium, indem sie durch horizontalen Gentransfer (HGT) zusätzliche DNA-Stücke in das Bakterium einführten. Beim HGT nimmt ein Bakterium DNA auf, die in der Umgebung – in diesem Fall im Reagenzglas – frei herumschwimmt. Diese DNA-Stücke enthielten Gene, die von anderen Bakterienarten dazu genutzt werden, Xylose zu verarbeiten. Sie dienten dem Bakterium P. putida sozusagen als Anleitung, wie Xylose verstoffwechselt werden muss. Dann gaben die Forschenden dem manipulierten Bakterium Xylose als Nahrungsquelle und warteten darauf, dass zumindest einige der P. putida Bakterien der vorgegebenen Anleitung folgen konnten.
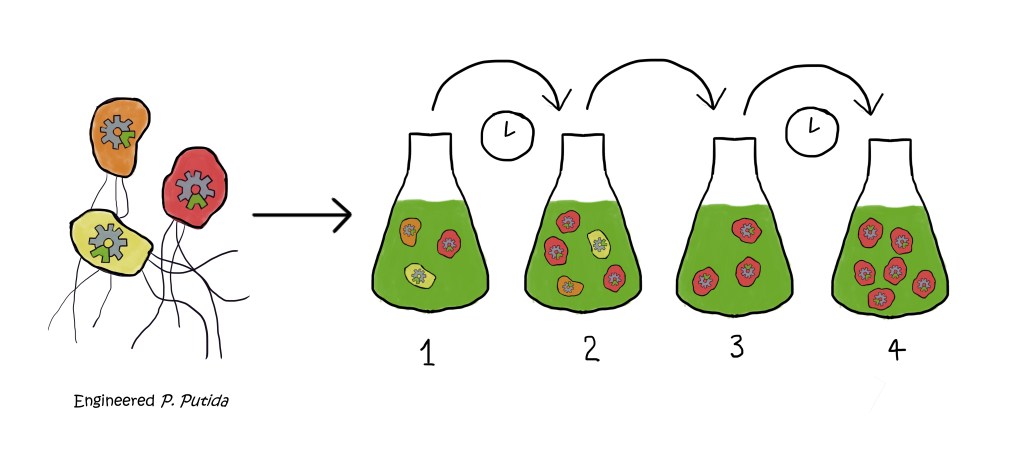
Aber wenn ein Bakterium ein neues DNA-Stück erhält, ist es anfangs überfordert und benötigt ein bisschen Zeit, um seinen Stoffwechsel umzustellen. Einigen Bakterien fällt es schwerer, den Anleitungen zu folgen als anderen. Und genau hier kommt dann das Prinzip des „Überlebens des am besten angepassten Individuums“ ins Spiel: Einige der Bakterien erwerben zufällig neue Mutationen, die ihnen dabei helfen, in der neuen Umgebung zu überleben oder sich an die neuen DNA-Stücke zu gewöhnen. Mit der Zeit gewinnen die Bakterien die Oberhand, die am besten angepasst sind. Sie vermehren sich und bringen schlussendlich ein Bakterium hervor, das Xylose ohne Probleme verstoffwechseln kann.
Die Forschenden nutzten dann noch viele weitere Labor- und Computermethoden, um zu verstehen, was im Inneren der Bakterien bei der Umstellung von Glukose auf Xylose genau geschehen war. Diese Erkenntnisse können in der Zukunft verwendet werden, um die Ernährungsumstellung von Bakterien noch weiter zu beschleunigen.
Link to the original post: Dvořák, P., Burýšková, B., Popelářová, B. et al. Synthetically-primed adaptation of Pseudomonas putida to a non-native substrate D-xylose. Nat Commun 15, 2666 (2024). https://doi.org/10.1038/s41467-024-46812-9
Featured image: Illustrated by Michaela Krupová using Krita 5.0.6
Übersetzt von: Ann-Kathrin Mehnert