20 woorden voor de hoofdpagina

Microbiologie in hapklare porties
Kleine dieren, grote conclusies.
Het verband bepalen tussen de samenstelling van onze darmflora en de oorzaak of het verloop van chronische ziekten is een hele uitdaging. Wetenschappers proberen al tijden om een verband te leggen tussen bepaalde ziektes en microben. Hiervoor worden onder andere menselijke microbioom-geassocieerde knaagdier-modellen voor gebruikt (EN: Human Microbiota Associated (HMA) murine models).
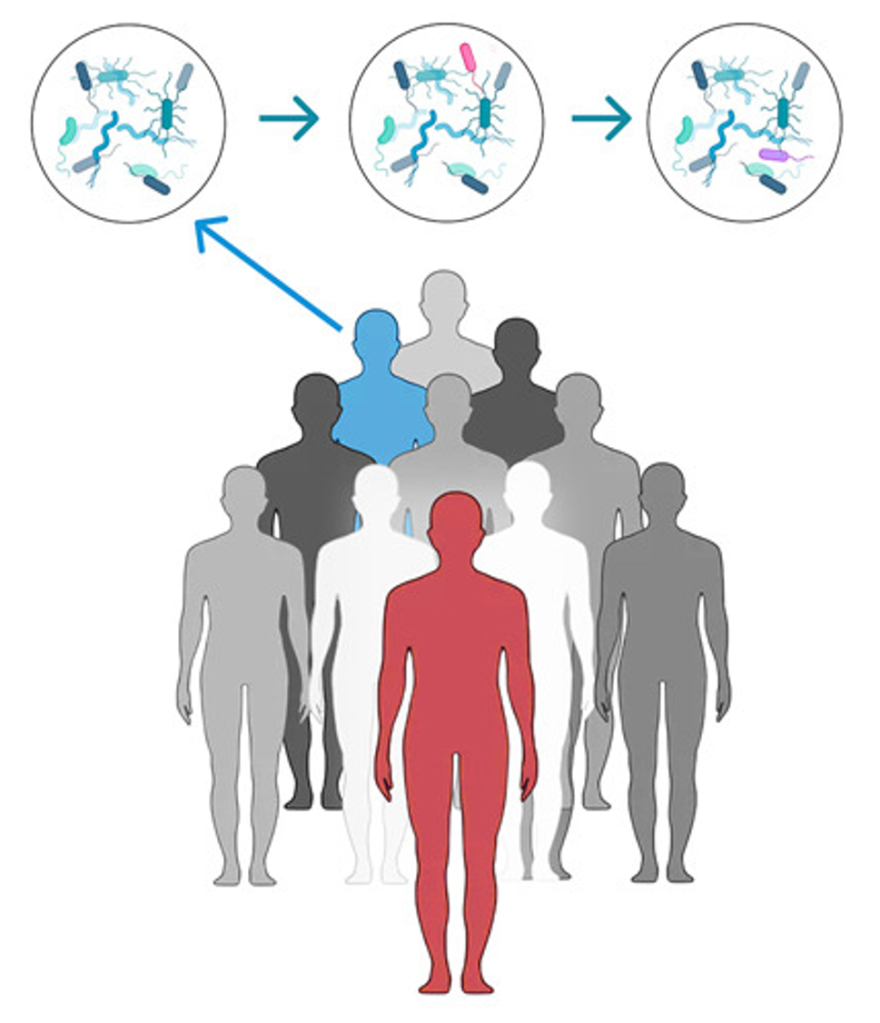
Deze HMA-modellen zijn veelal microbe-vrije muizen die opgegroeid zijn in een steriele omgeving. De knaagdieren krijgen ontlasting van gezonde vrijwilligers en/of patiënten die gediagnosticeerd zijn met een chronische ziekte. Als de ziekte verschijnt in de muis na deze zogenoemde ‘transplantatie’, dan is is er sprake van een oorzakelijk verband. Helaas is dat alles wat er over deze methode kan worden gezegd, want er is nog geen standaard methode ontwikkeld om experimenten uit te voeren die gebruik maken van dit dierlijk model.
De voor- en nadelen van de methode werd onderzocht door Jens Walter en collega’s in een systematisch onderzoek van 38 eerdere studies.
De auteurs noemen eerst de voordelen van de HMA-modellen:
- Een HMA model geeft inzicht in het ontstaan en het verloop van de ziekte in knaagdieren die de ontlasting hebben ontvangen, en alle omgevingsfactoren (eten, temperatuur etc.) zijn door onderzoekers precies te controleren.
- De onderzoekers kunnen goed de verschillen bekijken tussen de knaagdieren die gezonde ontlasting hebben gekregen en knaagdieren die ontlasting van een zieke patiënten hebben gekregen.
- Het is makkelijk om DNA-sequencing technologieën toe te passen in de experimenten (zoals het sequencen van het metagenoom), om te kijken naar de verschillen tussen de bacteriesamenstelling in de darmen van de knaagdieren.

Deze muismodellen zouden ons dus in staat moeten stellen om verbanden te kunnen leggen tussen het microbioom van onze darmen en bepaalde ziekten. Toch leggen de auteurs nadruk op enkele beperkingen van het model, en geven suggesties om dit te verbeteren.
Integriteit van de darmflora van de donoren.
Microben van menselijke donoren zijn niet altijd in staat om ook de darmen van de knaagdieren te koloniseren. De bacteriesoorten die wel in de darm blijven overleven leggen de basis voor een geheel andere bacteriesamenstelling. Zo wijzen de auteurs op studies waarin de samenstelling van het microbioom in de knaagdieren anders was dan in de oorspronkelijke donor. Gek genoeg concluderen dezelfde studies toch dat ze positieve associaties hadden gevonden tussen het microbioom en de ziekte die werd onderzocht. Het is dus belangrijk om na te gaan of de bacteriesamenstelling in de knaagdieren voldoende representatief is voor de oorspronkelijke bacteriesamenstelling van de menselijke donor.
De knaagdiermodellen zelf.
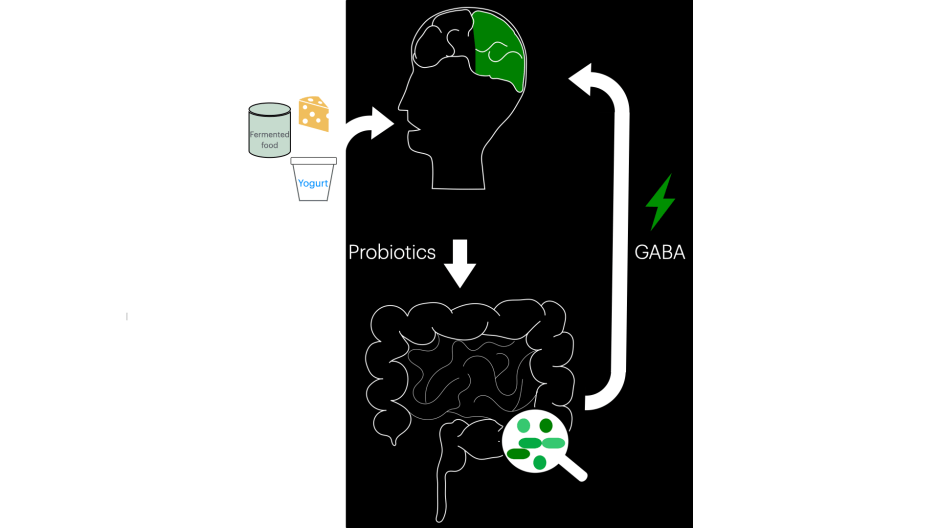
Het is aangetoond dat onze darmflora een belangrijke rol speelt bij de ontwikkeling van zowel ons immuunsysteem als het zenuwstelsel. Aangezien de knaagdieren zijn grootgebracht in een steriele omgeving, zijn ze meer vatbaar voor immunologische en neurologische problemen. Bovendien verschilt het immuunsysteem van knaagdieren met dat van mensen, en zijn daarom – als je het verband tussen microben en auto-immuunziekten zou bestuderen – geen ideale modellen. Dit probleem kan worden aangepakt als de knaagdieren worden ‘gehumaniseerd’ (dan worden er humane immuuncellen toegediend). Ook kan er misschien gebruik worden gemaakt van andere dierlijke modellen waarvan het immuunsysteem beter overeenkomt met dat van mensen, zoals apen of varkens.

Homogeniseren van heterogene ziekten.
De methoden voor het ontwerpen van experimenten gebaseerd op het HMA-model variëren sterk. Het microbioom van iedere persoon is uniek, net zoals onze vingerafdruk. Desondanks zijn er enkele onderzoeken die de stalen van de donoren hebben samengevoegd voor transplantatie in knaagdieren. Daardoor kunnen individuele kenmerken die mogelijk verband hielden met de status of de ernst van de ziekte niet opvallen. Daarom is het belangrijk om ervoor te zorgen dat er voldoende donoren zijn om de biologische variatie in de kliniek nauwkeurig weer te geven.
Meten is weten.
Een andere factor zijn de statistische gevolgen van het samenvoegen van de donor-stalen. Meer knaagdieren dan menselijke donoren leveren een vertekend beeld van welke ziektes door een bacterie worden veroorzaakt. Een voorbeeld: Als in werkelijkheid maar een paar mensen met de ziekte een grote hoeveelheid van bacteriesoort A hebben, maar deze stalen worden samengevoegd met andere stalen (die geen grote hoeveelheid van bacterie A bevatten), dan zouden de resultaten van het experiment erop wijzen dat alle mensen met de ziekte een grote hoeveelheid van bacterie A hebben. Het is dus statistisch nauwkeuriger om eenzelfde hoeveelheid donoren en proefdieren te hebben.
Uiteindelijk is het HMA-knaagdiermodel niet de enige manier om oorzakelijke verbanden te bestuderen. Zowel vooruitgang in statistische modellen als het rechtstreeks aanpassen van de menselijke darmflora zijn veelbelovende methoden om de koppeling van onze darmflora en bepaalde ziektes beter te begrijpen. Een combinatie van deze nieuwe technieken (en waar nodig het gebruik van de ‘klassieke’ HMA-modellen) kan microbioom-onderzoek een stevige impuls geven.
Link naar het originele artikel: Walter J, Armet AM, Finlay BB, Shanahan F. Establishing or exaggerating causality for the gut microbiome: lessons from human microbiota-associated rodents. Cell. 2020 Jan 23
Vertaald door: Charlotte van de Velde