Microbiologie in hapklare porties
De dood van Bacillus subtilis geeft aanleiding tot nieuwe celstructuren.
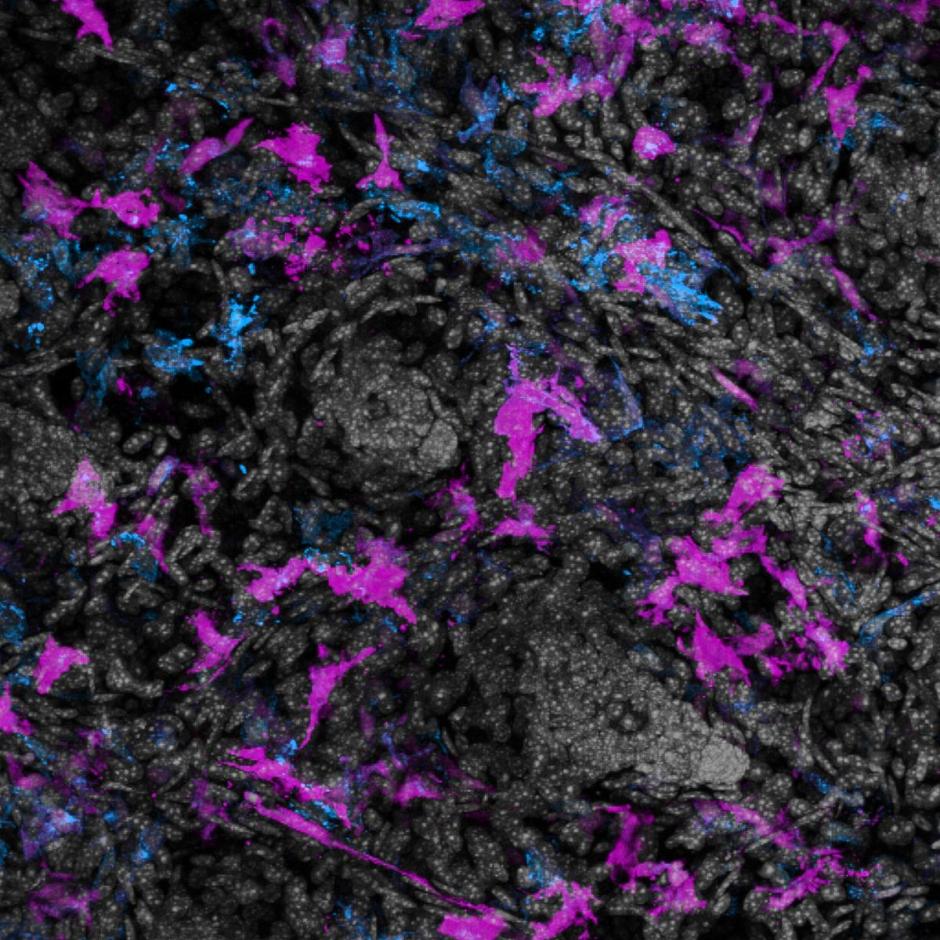
Ondanks hun eenvoudige structuur blijven bacteriën wetenschappers verbazen door hun eigenaardige mechanismen om zich aan te passen en te overleven. Pili en flagella zijn de meest bekende, en waarschijnlijk ook de meest bestudeerde bacteriële structuren. Om het geheugen even op te frissen: pili zijn korte, haarachtige structuren verantwoordelijk voor de hechting aan oppervlakken. Sommige soorten pili zijn zelfs betrokken bij bacteriële celdeling. Flagella daarentegen zijn stijve structuren die bij veel bacteriën voor de beweeglijkheid zorgen. Maar heb je ooit gehoord van nanobuisjes? Ze worden aangetroffen in de bacterie Bacillus subtilis, en in tegenstelling tot de pili en falgella, bestaan deze structuren uitsluitend uit lipiden (vetten) die een cytoplasmatisch membraan vormen. Dit is vrij zeldzaam voor een organel, maar het zorgt voor een grotere flexibiliteit én snellere assemblage/constructie.
In het geval van B. subtilis treffen we twee soorten nanobuisjes aan: Uitbreidende nanobuisjes zijn verantwoordelijk voor het vergroten van het oppervlak van een cel, waardoor bacteriën (meer) voedingsstoffen uit de omgeving kunnen opnemen. Intercellulaire nanobuisjes creëren een verbinding tussen cellen. Deze verbinding kan plaatsvinden tussen twee (verschillende) bacteriesoorten of zelfs tussen bacteriën en eukaryote cellen.
Pospíšil en collega’s hebben een studie uitgevoerd waarin ze genen en de factoren in de omgeving hebben onderzocht die noodzakelijk zijn voor de vorming van nanobuisjes in B. subtilis. Bij het woord “buisjes” zou je denken dat deze structuren verantwoordelijk zijn voor het transport van voedingsstoffen en/of genetisch materiaal. Bacteriën leven immers in gemeenschappen, waarin cellen de hulpbronnen (nl. voedingsstoffen en genetisch materiaal) delen.
Nu blijkt echter dat nanobuisjes alleen vormen onder (cellulaire) stress-omstandigheden. Belangrijker nog is dat deze structuren ontstaan tijdens of na celdood. Ze dienen niet als transportkanalen, maar zijn een teken van uiteenvallende cellen. Deze conclusie werd getrokken na een experiment, waarbij de onderzoekers een dekglaasje tegen bacteriën drukten om een monolaag te maken (een enkele laag die één cel dik is). Het uitoefenen van druk met een dekglaasje is voldoende om een stressreactie in bacteriën op te wekken en de productie van nanobuisjes in gang te zetten. Maar hoeveel tijd neemt dit proces in beslag? Het antwoord zal je misschien verbazen. Het duurt slechts enkele seconden voordat deze nanobuisjes zich hebben geassembleerd en verschijnen! Zodra de onderzoekers een afname van het signaal uit het celmembraan registreerden, nam de productie van nanobuisjes toe. Daarom werd aangenomen dat zodra cellen beginnen af te sterven en uit elkaar vallen, de ontstane lege plekken worden gebruikt om de nanobuisjes in te laten groeien.
Om het mysterie van de bacteriële nanobuisjes tot op de bodem uit te zoeken, bestudeerden de onderzoekers de genetische mechanismen achter de vorming van deze structuren. Wanneer een bacteriecel stress ervaart, past hij zich aan de omstandigheden aan of sterft hij wanneer de stress te groot is. Wanneer een cel er niet in slaagt zich aan de stressomstandigheden aan te passen, wordt de transcriptiefactor SigD essentieel. Met behulp van een groep genen, de zogenaamde CORE-element genen, versnelt deze factor het proces van gen-transcriptie. Bovendien zijn nanobuizen, zoals eerder gezegd, opgebouwd uit lipiden en niet uit eiwitten zoals de rest van de organellen in een cel. Om de celwand te verzwakken en af te breken zijn de autolysines LytE en LytF nodig. Autolysines zijn enzymen die de bestanddelen van bacteriële cellen afbreken.
Interessant genoeg zijn er andere bacteriesoorten die soortgelijke structuren bezitten(bijvoorbeeld een andere vertegenwoordiger van het Bacillus-geslacht Bacillus megaterium, of Escherichia coli). En nogmaals, deze organismen hebben een of andere stressfactor nodig om de vorming van nanobuisjes te induceren. Hoewel de auteurs van het artikel concluderen dat nanobuisjes van B. subtilis een kenmerk zijn van stervende of dode cellen, haasten zij zich niet om hetzelfde aan te nemen voor andere bacteriesoorten. Ze concluderen dat meer onderzoek nodig is om de fysiologische rol van nanobuisjes in andere organismen te weten te komen.

Link to the original post: Pospíšil, J., Vítovská, D., Kofroňová, O. et al. Bacterial nanotubes as a manifestation of cell death. Nat Commun 11, 4963 (2020).
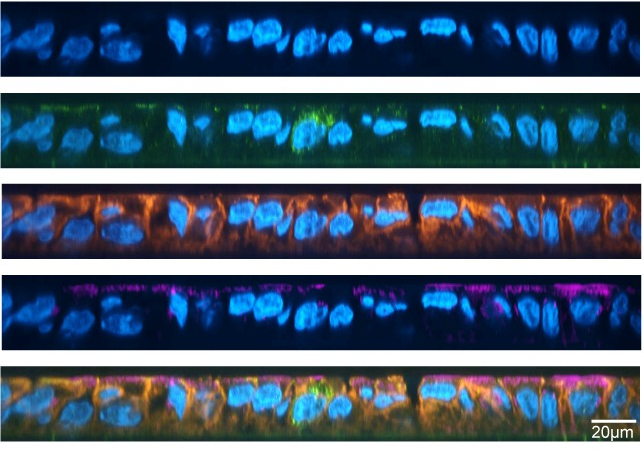
Featured image: https://www.nature.com/articles/s41467-017-00344-7/figures/3
Vertaald door: Charlotte van de Velde