Microbiologie in hapklare porties
Microben en immuuncellen in de strijd tegen antibioticaresistentie.
Antibiotica zijn chemische stoffen die micro-organismen kunnen vernietigen (bactericide antibiotica), of de groei ervan kunnen verhinderen (bacteriostatische antibiotica) [1]. Toen Alexander Fleming in 1928 Peniciline ontdekte, werd het gouden tijdperk van de antibiotica – het wonderwapen in de strijd tegen besmettelijke ziekten – ingeluid [2]. Maar naarmate de populariteit toenam, steeg ook het risico dat pathogenen (ziekteverwekkers) resistentie zouden ontwikkelen. Dit risico werd een feit, en pathogenen beschikken tegenwoordig over een arsenaal aan verdedigingsmechanismen tegen bijna alle beschikbare antibiotica die hun voortbestaan bedreigen [1]. Dit fenomeen noemen we antibioticaresistentie. Als reactie op de toenemende antibioticaresistentie bij pathogenen en de daaropvolgende antibioticacrisis, bundelen internationale gezondheidsorganisaties en onderzoekers over de hele wereld nu hun krachten om deze crisis aan te pakken.
Waar vinden we pathogenen en wat veroorzaken ze?
Pathogenen bevinden zich op verschillende plaatsen in het lichaam, of op plaatsen daarbuiten waar ze makkelijk het lichaam kunnen binnendringen. We vinden ze op de huid, of in de longen, het darmstelsel of bloed. Deze pathogenen veroorzaken ziekten zoals urineweginfecties, longontstekingen en sepsis [3].
Klebsiella pneumoniae is een van de pathogenen die algemeen wordt aangetroffen in de darm en kan levensbedreigende infecties veroorzaken. De antibiotica-resistente variant van deze pathogeen vindt men tegenwoordig overal ter wereld en zelfs de sterkste antibiotica blijken niet langer doeltreffend [4].
Waarom voorkomen we dan niet gewoon de infectie en verspreiding van Klebsiella pneumoniae?
Hiervoor moeten we weten welke factoren bijdragen tot een succesvolle infectie en kolonisatie. Dit leidt ons tot vragen over de relatie tussen het microbioom, de immuniteit van de gastheer én het resultaat van de infectie.
Onlangs ontdekten Sequeira en collega’s twee nieuwe mechanismen waarmee bacteriën in het microbiota van de gastheer diens de immuniteit kunnen activeren om K. pneumoniae infectie te voorkomen [5]. Laten we even verder inzoomen op deze verdedigingsmechanismen…
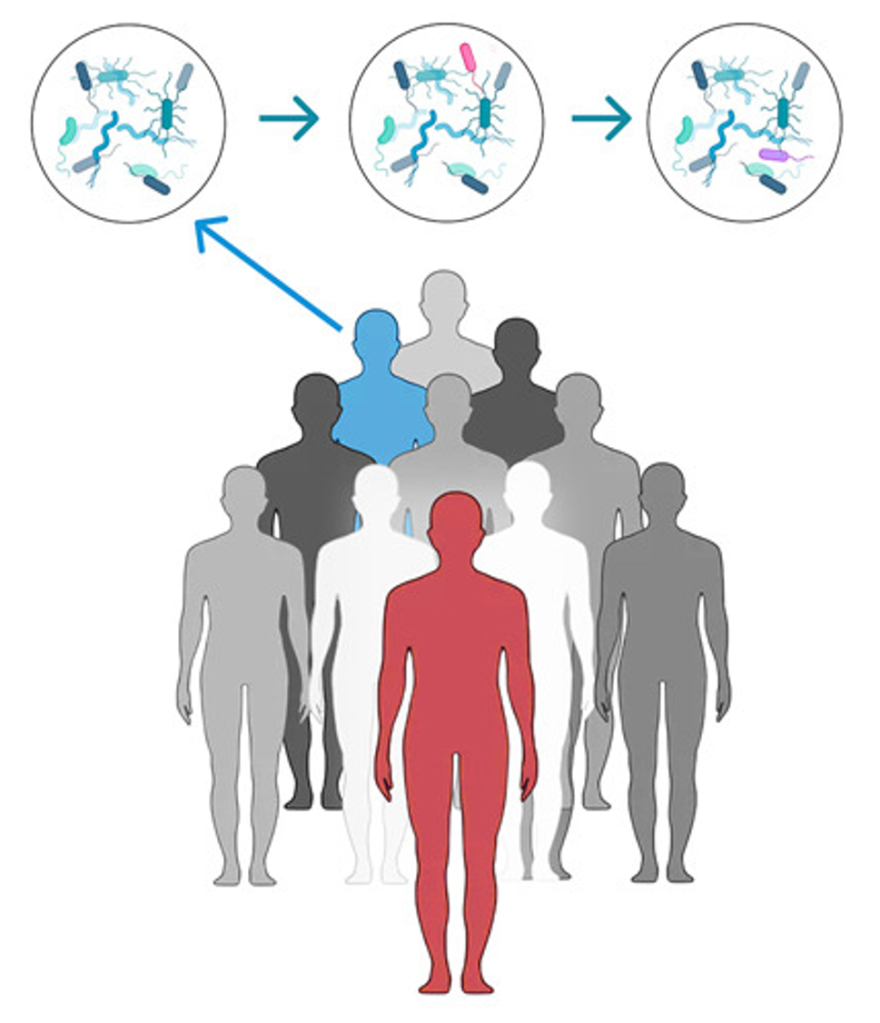
De menselijke microbiota bevat verschillende micro-organismen, afhankelijk van de plaats van het lichaam. Neem bijvoorbeeld de Bacteroidetes-soorten die we (in hun niet-pathogene vorm) aantreffen in de darm en wiens genoom een commensale kolonisatiefactor (CKF) locus kan bevatten. In aanwezigheid van zo’n CKF produceren Bacteroidetes een beschermende polysaccharide-capsule. Hierdoor ontstaat er een interactie met het darmslijmvlies (de intestinale mucosa), die resulteert in een activatie van het aangeboren immuunsysteem [5]. Specifiek wordt de macrofaag-respons in gang gezet, resulterend in een verhoogde secretie van IL-36𝛄. IL-36 is een pro-inflammatoir cytokine (een signaalmolecuul) dat bij binding aan zijn receptor een signaalcascade activeert die voorkomt dat K. pneumoniae de darm koloniseert (Figuur 1, links). Echter, deze IL-36 signalering is afhankelijk van macrofagen. De afwezigheid van deze macrofagen of de CKF locus in de Bacteroidetes resulteerde dan ook in een (verhoogde) gevoeligheid voor K. pneumoniae [6].

In de bovenste luchtwegen daarentegen, lijken niet Bacteroidetes maar Proteobacteria de graad van bescherming tegen K. pneumoniae te bepalen [5]. Zij doen dit via IL-17A cytokine signalering, meer bepaald door de homeostatische IL-17A productie in de bovenste luchtwegen te herstellen. Als gevolg hiervan kon de kolonisatie van niet-ingekapselde K. pneumoniae worden voorkomen in aanwezigheid van Proteobacteria [6]. Maar de bescherming faalde echter voor ingekapselde K. Pneumoniae, die met succes de bovenste luchtwegen koloniseerde (Figuur 1, rechts).
Waar Bacteroidetes inkapseling gebruiken als bescherming tegen K. pneumoniae-kolonisatie in de darm, gebruikt K. Pneumoniae inkapseling om de bescherming van Proteobacteria in de bovenste luchtwegen te weerstaan. Wanneer Anti-IL-17A werd toegediend om de cytokine signalering te verstoren, werden er enkel nog ingekapselde K. pneumoniae gevonden, en geen vrije (niet ingekapselde) pathogenen [6]. Dit wijst erop dat K. Pneumoniae in staat is om verdedigingsmechanismen te ontwikkelen gebaseerd op zijn (in)directe omgeving – hier Bacteroidetes versus Probacteria en darm versus bovenste luchtwegen.
Kortom, de auteurs toonden aan dat de microbiota van de gastheer bescherming kan bieden tegen kolonisatie door antibiotica-resistente K. pneumoniae in de darm, maar niet in de bovenste luchtwegen. Dit wijst erop dat pathogenen beroep kunnen doen op verschillende virulentiestrategieën (i.e. manieren om de immuunrespons van de gastheer te omzeilen) afhankelijk van de de plaats in het lichaam. Inzicht in de interactie tussen pathogenen en hun directe omgeving kan bijdragen tot de ontwikkeling van nieuwe antimicrobiële strategieën als alternatief voor de overmatig gebruikte antibiotica. Door deze studies uit te breiden naar andere klinisch relevante pathogenen, – bijvoorbeeld diegenen geassocieerd met multi-drug resistente infecties – kunnen gemeenschappelijke mechanismen van kolonisatieresistentie onderzocht worden en patronen in de interactie van pathogenen, microbioom, en het immuunsysteem geïdentificeerd..
Link to the original post: Sequeira, R. P., et al. (2020). “Commensal Bacteroidetes protect against Klebsiella pneumoniae colonization and transmission through IL-36 signalling.” Nat Microbiol 5(2): 304-313.
Other references:
- Aminov, R. I. (2009). “The role of antibiotics and antibiotic resistance in nature.” Environ Microbiol 11(12): 2970-2988.
- Hutchings, M. I., et al. (2019). “Antibiotics: past, present and future.” Curr Opin Microbiol 51: 72-80.
- CDC – Healthcare-associated Infections – Homepage. https://www.cdc.gov/hai/index.html September 12, 2021
- WHO – Antimicrobial Resistance – Homepage. https://www.who.int/news-room/fact-sheets/detail/antimicrobial-resistance September 12, 2021
- Solis, A. G. and M. Levy (2020). “The biogeography of colonization resistance.” Nat Microbiol 5(2): 234-235.
- Sequeira, R. P., et al. (2020). “Commensal Bacteroidetes protect against Klebsiella pneumoniae colonization and transmission through IL-36 signalling.” Nat Microbiol 5(2): 304-313.
Featured image: Credit: Darryl Leja, NHGRI on Flickr
Vertaald door: Lieselotte Peeters