Microbiologie in hapklare porties
De prokaryote oorsprong van onze grootste methode voor genetische modificatie.
CRISPR is tegenwoordig de gouden standaard in genetische modificatie. Het is sneller, goedkoper en efficiënter dan concurrerende methoden. Wetenschappers hebben vastgesteld dat CRISPR gebruikt kan worden om de genomen van planten en dieren (waaronder mensen) aan te kunnen passen [1]. “Gentherapie” zou bijvoorbeeld erfelijke ziekten kunnen aanpakken, of veroudering tegengaan. Zo gebruikten Chinese onderzoekers CRISPR om het gen CCR5 in een tweeling te veranderen [2]. Door CCR5 kunnen mensen met HIV worden besmet, dus het veranderen ervan zou tegen het virus kunnen beschermen. Dit voorbeeld toont de moderne toepassingen van CRISPR. Maar waar komt CRISPR eigenlijk vandaan? Anders dan het gebruik in menselijke cellen doet vermoeden, vindt dit moleculaire gereedschap zijn oorsprong in prokayoten.
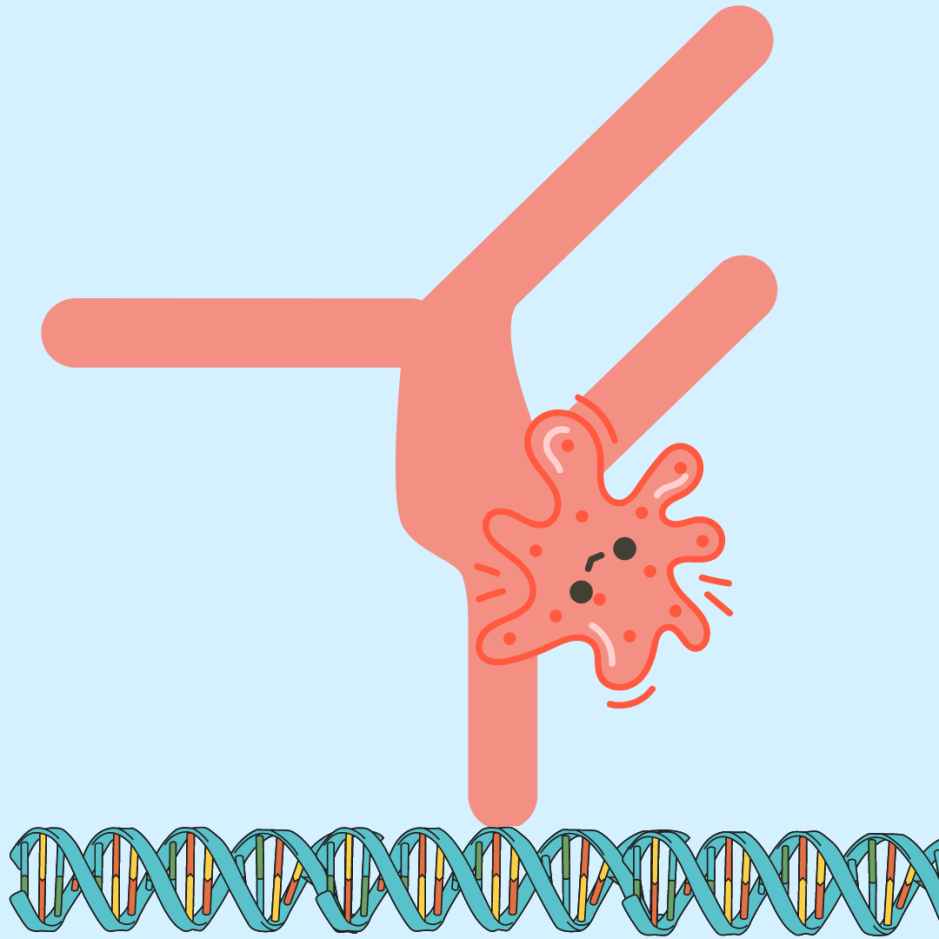
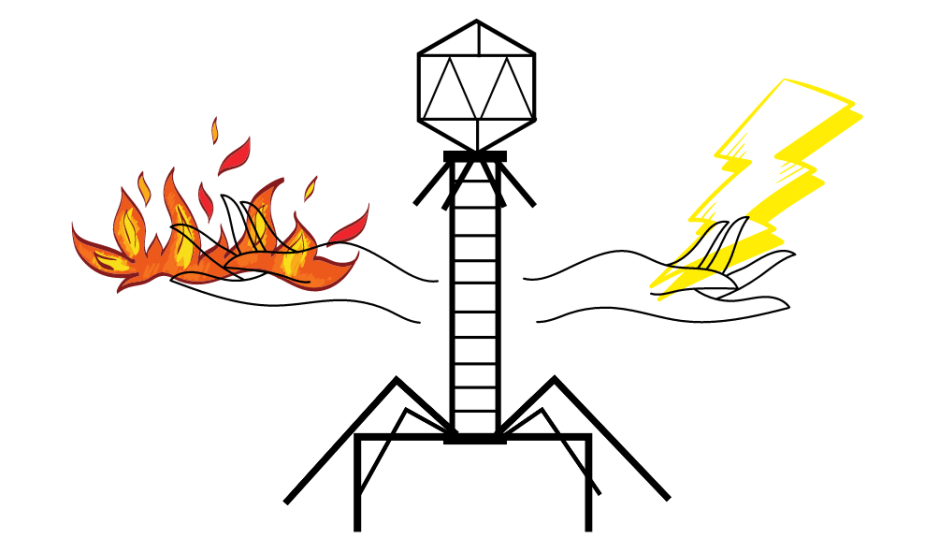
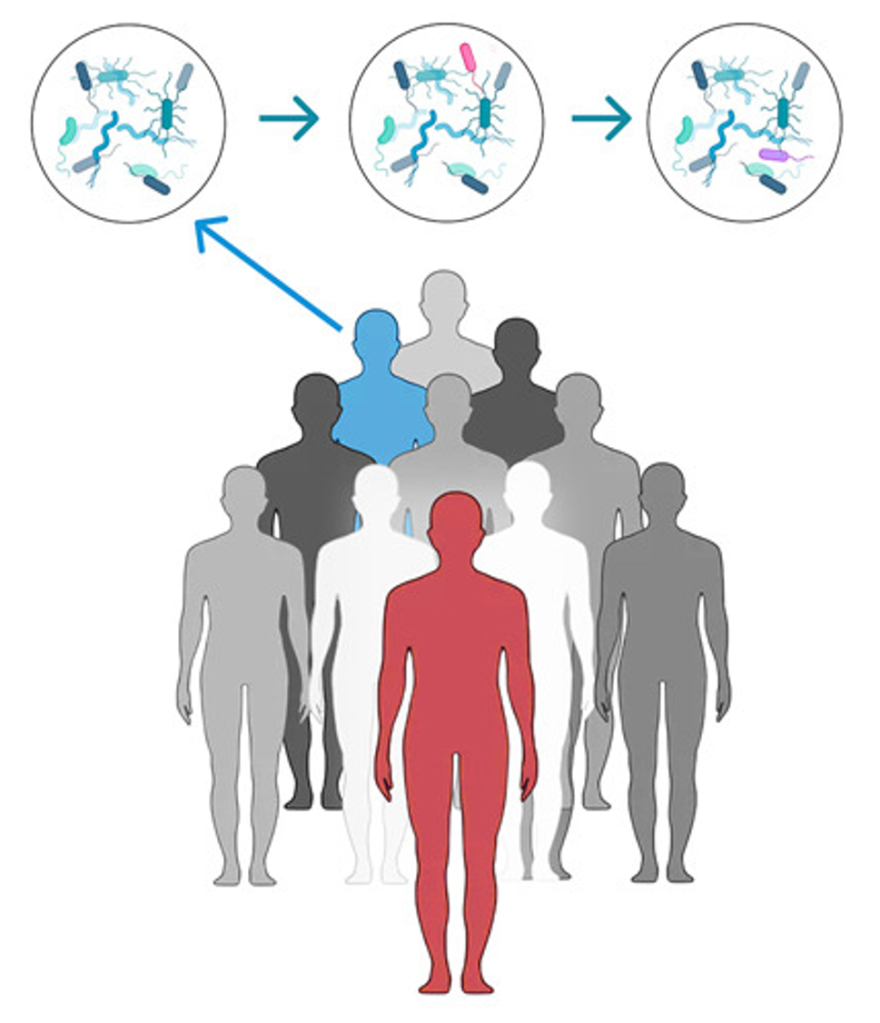
CRISPR is een reactief “immunsysteem” van prokaryoten. Bacteriën en archaea zijn voortdurend het doelwit van ‘fagen’, een type virussen. Ter bescherming dient onder andere CRISPR – een Engelse afkorting voor Clustered Regularly Interspaced Short Palindromic Repeats. Een specifieke regio in het prokaryoot genoom, het CRISPR locus, bevat veel kopieën van dezelfde sequentie. Deze repeat-sequenties worden afgewisseld met variabele stukjes DNA die spacers heten (Figuur 1A) [3]. Deze spacers zijn stukjes DNA van een virus die in het verleden door de prokaryoot verslagen is. Net als ons eigen immuunsysteem informatie van de vorige indringers opslaat, vormt CRISPR het “moleculair geheugen” van virale aanvallen. Het voordeel van zo’n geheugen is dat het genetisch materiaal van een ongewenste bezoeker snel herkend én vernietigd kan worden.

Het bestaan van CRISPR-sequenties werd voor het eerst in 1993 gerapporteerd door Francisco Mojica [1]. De biologische functie van de locus was toen nog onbekend. Bijna twintig jaar later toonden onderzoekers van het bedrijf Danisco in Kopenhagen de functie van CRISPR aan: een immuunsysteem tegen fagen [3]. De zuivelindustrie inversteerde flink in het begrijpen van het bacterieel immuunsysteem, omdat de productie van veel zuivelproducten door fagen heftig aangetast kan worden. Danisco’s Rodolphe Barrangou en Phillipe Horvath toonden experimenteel aan dat CRISPR-sequenties een bacterie immuun maken voor fagen die homologe (dezelfde) sequenties in hun eigen genoom hebben [3].
Voor hun onderzoek gebruikten Barrangou en Horvath Streptococcus thermophilus, een melkzuurbacterie die veel in de zuivelindustrie wordt gebruikt. Bacterie-stammen binnen deze soort die meer resistentie tegen fagen vertoonden, bleken meer verschillende spacers in hun CRISPR-locus te hebben. Dat wees erop dat CRISPR iets met immuniteit te maken had [3].
Hoe krijgt S. thermophilus de spacers in zijn genoom? De studie toonde aan dat CRISPR-loci een dynamisch deel van het genoom zijn, dat snel verandert tijdens faag-aanvallen [3]. Dit onderzochten de Denen door een bacteriestam met een zwak immuunsysteem bloot te stellen aan “faag #858”, die ze in een beker yoghurt hadden gevonden. Door de overlevende bacteriën op te kweken, maakten de onderzoekers hun eigen 858-resistente S. thermophilus. Alle overlevers bleken in het CRISPR-locus extra stukken DNA te hebben. Deze stukken waren allemaal fragmenten uit het faag 858-DNA. De homologie tussen spacer en infecterend DNA leek dus doorslaggevend voor de immuniteit van de bacterie.
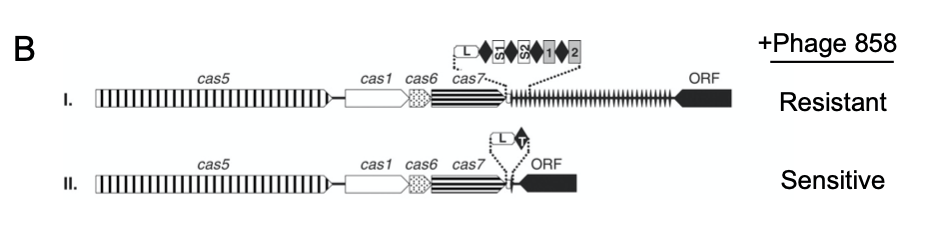
Om te toetsen of die theorie klopt, knipten Barrangou en Horvath de spacers van een 858-resistente bacteriestam en plakte die op dezelfde plaats in een 858-gevoelige stam (Figuur 1B). Het resultaat: de gemodificeerde stam bleek resistent geworden tegen faag 858! De truc werkte andersom ook: door de spacer die homologie vertoonde met faag 858 te verwijderen, kon een resistente bacterie ineens wél geïnfecteerd worden door faag 858. De spacers bieden dus een zeer gerichte immuniteit [3].
Spacers zijn niet de enige elementen in het immuunsysteem CRISPR. Ook de cas-genen, die recht naast de CRISPRs zitten, zijn voor virale immuniteit van belang. Sinds de ontdekking van Barrangou en Horvath hebben baanbrekende onderzoeken de rollen van deze genen blootgelegd [1]. Door het grote plaatje van CRISPR te begrijpen kon het omgebouwd worden tot laboratorium-werktuig. Zo bracht een bacteriëel immuunsysteem een explosie van nieuwe toepassingen in de biotechnologie en geneeskunde!
Literature Cited
- Lander, E.S. (2016). The Heroes of CRISPR. Cell 164, 18-28.
- Raposo, V.L. (2019). The First Chinese Edited Babies: A Leap of Faith in Science. JBRA Assist Reprod. 23, 197-199.
- Barrangou, R., Fremaux, C., Deveau, H., Richards, M., Boyaval, P., Moineau, S., Romero, D.A., and Horvath, P. (2007). CRISPR provides acquired resistance against viruses in prokaryotes. Science 315, 1709–1712.
Featured image: https://i1.wp.com/foodcrumbles.com/wp-content/uploads/2018/07/Home-made-yogurt-1-2.jpg?fit=750%2C500&ssl=1
Vertaald door: Steven Pilon