Microbiologie in hapklare porties
Een eenvoudige omschakeling van vriend naar vijand.
De wereld rondom ons krioelt van de micro-organismen, van in de oceaan tot in onze eigen darmen. Microben worden over het algemeen bestempeld als pathogeen, maar in de realiteit is dit slechts een klein gedeelte ervan. Veel microben leven vreedzaam zonder schade te brengen aan ons of aan andere levende wezens; ze kunnen zelfs voor voordelen zorgen bij hun gastheer door ze te beschermen of te bevoorraden met essentiële voedingsstoffen.
Wat maakt pathogenen dan effectief pathogenen?
De sleutel voor een microbe om zijn gastheer te infecteren vinden we terug in zijn genoom. Pathogenen beschikken over een verzameling door hun genen gecodeerde hulpmiddelen om een gastheer aan te vallen of de immuunafweer van de gastheer te omzeilen. Commensale microben bezitten deze genen over het algemeen niet, of als ze die wel hebben, dan uiten ze deze niet. Andere bacteriën, ook wel gekend als opportunistische pathogenen, kunnen naadloos omschakelen van een onschuldige vriend naar een besmettelijke vijand.
Veel wetenschappers voeren onderzoek naar deze opportunistische omschakeling in een bacterie genaamd Staphylococcus epidermidis. S. epidermidis is één van de vele microben die we gewoonlijk aantreffen op onze huid. Terwijl deze doorgaans goedaardig is, kan deze bacterie ook een problematische pathogeen zijn in ziekenhuizen. S. epidermidis groeit meestal op geïmplanteerde medische apparaten en infecteert af en toe zelfs het bloed, wat leidt tot levensbedreigende ziektes zoals sepsis. Het heeft ook resistentie verworven tegen een aantal antibiotica, waardoor behandeling ervan een voortdurende uitdaging is. Interessant om weten is dat S. epidermidis niet veel genen heeft die helpen om de gastheer rechtstreeks aan te vallen. In plaats daarvan vertrouwt het op genetische hulpmiddelen om langs de immuunreactie van de gastheer te sluipen, binnen te dringen en zich in de gastheer te vestigen.
Hoe verandert deze microbe van onschuldig op onze huid tot één die levensbedreigende infecties veroorzaakt?
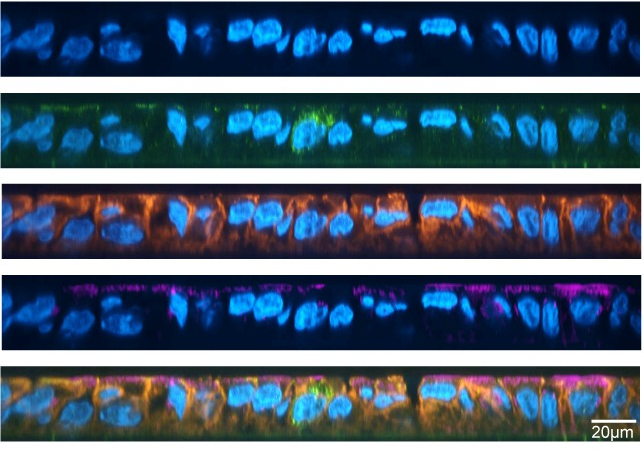
Eerder onderzoek door Dr. Laura Cau en anderen wees uit dat sommige S. epidermidis stammen van nature meer proteasen produceren, gekend als EcpA, dan anderen die leiden tot huidbeschadiging en ontsteking. Om meer te weten te komen over EcpA in S. epidermidis, lees The skin’s “frenemy”. In een recente studie heeft een groep onderzoekers uit Duitsland, Denemarken en China ontdekt dat stammen van S. epidermidis zijn omgeschakeld van een commensale naar een pathogene levensstijl met behulp van een complex suikermolecuul dat bekend staat als RboP wand-teichoïnezuur (WTA). WTA komt vrij veel voor in bacteriën en wringt zich tussen de peptidoglycaanlaag op de bacteriële celwand (Figuur 1).

Het speelt waarschijnlijk een cruciale rol in de manier waarop bacteriën hun vorm behouden, celprocessen controleren, en interageren met hun gastheer [2]. Alle stammen van S. epidermidis bezitten WTA, maar alleen pathogene stammen hebben RboP-WTA. De onderzoekers tonen aan dat RboP-WTA ervoor zorgt dat de besmettelijke S. epidermidis zijn gastheer kan koloniseren en hem in staat stelt sommige van zijn genetische hulpmiddelen te delen met Staphylococcus aureus, een pathogene verwant van S. epidermidis, om zijn nieuwe virulente levensstijl te verbeteren.
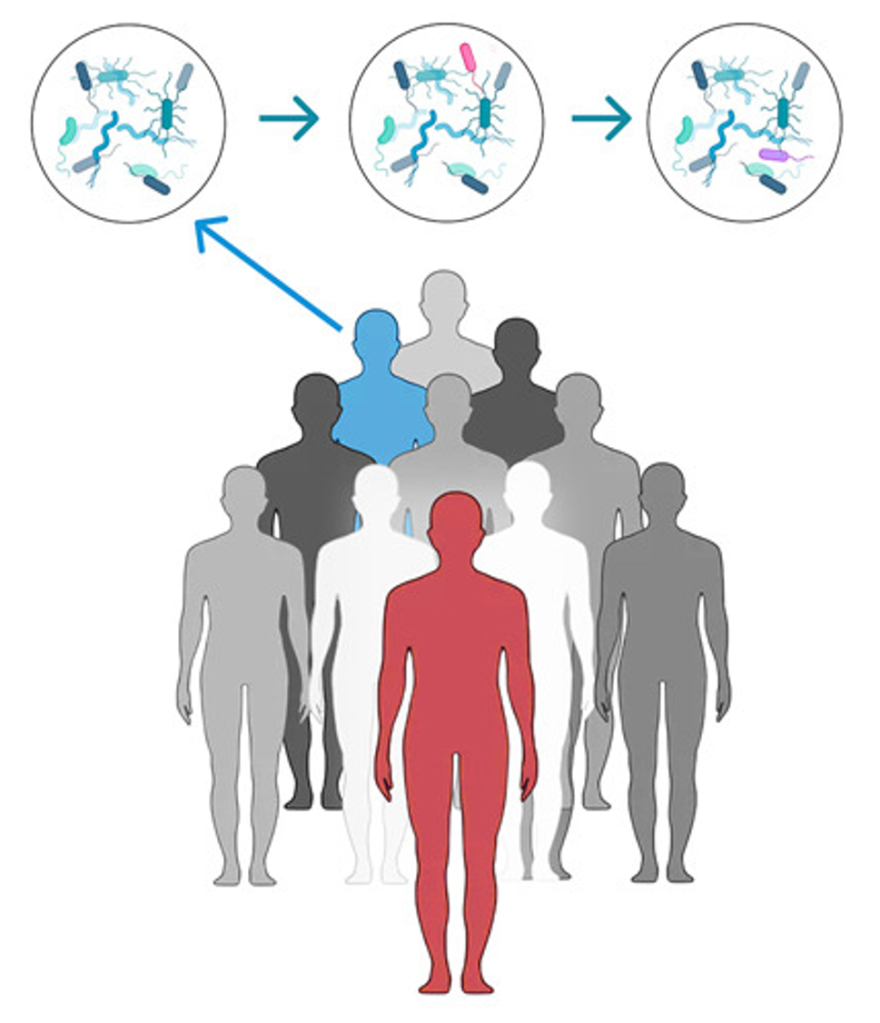
Het team van onderzoekers maakte gebruik van klinische stalen van S. epidermidis besmette patiënten om de belangrijkste verschillen te begrijpen tussen onschuldige en infectieuze stammen. Ze ontdekten dat pathogene S. epidermidis stammen twee types van WTA bezitten: GroP-WTA en RboP-WTA. Niet-pathogene S. epidermidis stammen hebben daarentegen enkel GroP-WTA (Figuur 2).

S. aureus bezit ook Rbo-WTA, wat suggereert dat RboP-WTA een pathogene levensstijl mogelijk maakt voor S. epidermidis. Verder onderzoek heeft aangetoond dat RboP-WTA de manier waarop de bacterie interageert en zijn gastheer koloniseert verandert. Volgens de studie infecteert S. epidermidis – die RboP-WTA tot expressie brengt – gemakkelijk de bloedbaan van de gastheer en verliest hij zijn vermogen om het epitheel van de gastheer te koloniseren zoals de commensale stammen.
Bacteriën werken vaak samen om te kunnen overleven en zich verder te ontwikkelen door waardevolle genen uit te wisselen. Aangezien S. aureus en de pathogene vorm van S. epidermidis allebei RboP-WTA bezitten, wilden de auteurs nagaan of deze twee soorten in staat zijn om DNA met elkaar uit te wisselen. Ze vonden dat alleen S. epidermidis stammen met RboP-WTA een groep van WTA-gerelateerde genen bezitten, die ervoor zorgen dat ze DNA kunnen uitwisselen met S. aureus. Bij de commensale S. epidermidis ontbreekt zowel de groep genen als de mogelijkheid om genetische informatie uit te wisselen met hun S. aureus verwanten. De auteurs veronderstellen dat de mogelijkheid van de pathogenen om DNA uit te wisselen met S. aureus, ervoor zorgt dat S. epidermidis kan leren hoe hij zijn gastheer beter kan aanvallen en hoe hij resistent kan worden voor de meest voorkomende antibiotica.
Deze bevindingen openen de deur naar het produceren van Staphylococcus vaccins, die RboP-WTA aanvallen zonder onze normale microflora te verstoren, wat een zeer grote stap is in het gevecht tegen antibiotica-resistente bacteriële pathogenen.
Als je meer wil te weten komen over deze soorten, kijk dan naar Danny Ward #52Species over Staphylococcus epidermidis!
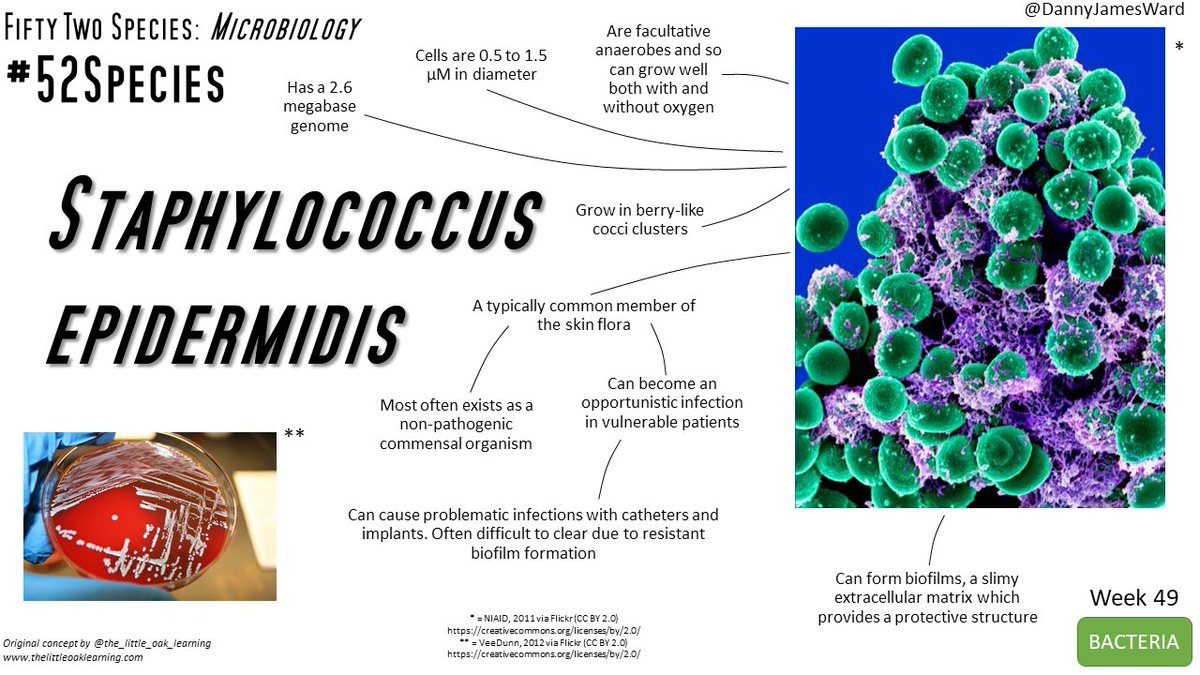
Originally tweeted by Danny Ward (@DannyJamesWard) on June 28, 2021.
Link to original article: Du, X., Larsen, J., Li, M. et al. Staphylococcus epidermidis clones express Staphylococcus aureus-type wall teichoic acid to shift from a commensal to pathogen lifestyle. Nat Microbiol 6, 757–768 (2021).
Other references:
- Cau, Laura et al. “Staphylococcus epidermidis protease EcpA can be a deleterious component of the skin microbiome in atopic dermatitis.” The Journal of Allergy and Clinical Immunology vol. 147 (2021): P955-966. doi:10.1016/j.jaci.2020.06.024
- Brown, Stephanie et al. “Wall teichoic acids of gram-positive bacteria.” Annual review of microbiology vol. 67 (2013): 313-36. doi:10.1146/annurev-micro-092412-155620
Featured image: Created with BioRender.
Written by Julie Starkey
Translated by Anke Van der Veken