Microbiologie in hapklare porties
Microben op dieet: hoe verander je de eetlust van bacteriën
Antibiotica. Insuline. Vitamine supplementen. Biobrandstoffen. Wasmiddelen. Wat hebben deze dingen gemeen? Ze worden allemaal gemaakt door microben. De biotechnologie-industrie gebruikt verschillende micro-organismen als piepkleine fabriekjes voor de grootschalige productie van veelgebruikte chemicaliën. De handel is relatief eenvoudig: ze geven ons wat we willen in ruil voor hun favoriete voedsel en omstandigheden die voor hen precies goed zijn om in te gedijen. Maar wat als hun favoriete snacks ook onze favorieten zijn? Kunnen we ze leren om in plaats daarvan iets anders lekker te vinden? Een internationale groep onderzoekers bestudeerde hoe een bacterie leert eten wat hij niet gewend is en hoe hij zijn metabolisme aanpast aan deze nieuwe maaltijd.
Microben met een zoetekauw
Microben die worden gebruikt in de biotechnologie-industrie zijn dol op suikers (en wie kan ze dat kwalijk nemen?). De universele favoriet lijkt glucose te zijn, die we gemakkelijk kunnen halen uit zetmeel (zetmeel is in feite een groot molecuul dat bestaat uit vele glucosemoleculen die in een keten met elkaar verbonden zijn). In de meeste gevallen komt het zetmeel uit producten zoals maïs, tarwe of aardappelen. Maar er zit een addertje onder het gras – dit zijn allemaal dingen die wij mensen ook lekker vinden. Wat als er een manier was om de microben te voeden met iets anders, iets dat mensen toch niet kunnen eten?
Nadat een maïsveld is geoogst, blijft er veel groene biomassa achter, zoals stengels en bladeren. Daar zitten ook veel suikers in, maar in een vorm die wij niet kunnen verteren. Als je op een maïsblad kauwt, komt het er aan de andere kant weer uit zonder dat het voedingsstoffen aan je lichaam heeft gegeven (waardoor je mogelijk een maagklachten krijgt). Als dit groene afval, dat we toch niet kunnen eten, gebruikt zou kunnen worden om de microben te voeden (en de lekkere producten voor ons over te laten), zou dat het hele proces goedkoper en duurzamer maken.
Een microbe leren zijn dieet te veranderen
Maar industriële microben voeden met groenafval in plaats van hun favoriete glucose is niet zo eenvoudig. Het vereist dat de microbe zijn metabolisme ‘herprogrammeert’ om andere suikers te kunnen eten, zoals xylose, een bestanddeel van het groenafval en na glucose de meest voorkomende monosacharide (enkelvoudige suiker) op aarde. Veel organismen die gebruikt worden in de biotechnologie kunnen zich niet voeden met xylose, terwijl andere het wel kunnen gebruiken, maar een sterke voorkeur hebben voor glucose. Een team wetenschappers van de Masaryk Universiteit in Praag, Tsjechië, heeft in samenwerking met onderzoekers uit Australië, Ierland, Duitsland en Spanje bestudeerd hoe de bacterie Pseudomonas putida, een van de meest gebruikte bacteriën in de biotechnologie, zich aanpast aan het eten van xylose.
Pseudomonas putida groeit snel en is relatief goedkoop in onderhoud, waardoor het een van de meest gebruikte minifabriekjes in de biotechnologie-industrie is. Omdat hij zo vaak wordt gebruikt, bestuderen onderzoekers hem vanuit alle mogelijke hoeken om hem zo goed mogelijk te begrijpen (bekijk een eerder bericht van maaikeloopt over hoe deze microbe omgaat met overbelasting). De onderzoekers in dit onderzoek wilden zien hoe een microbe leert om te eten wat hij niet gewend is, en omdat P. putida zich van nature niet kan voeden met xylose, was het een perfect organisme om deze vraag te beantwoorden. Eerder had een andere groep wetenschappers deze bacterie zo gemanipuleerd dat hij xylose kon opnemen, maar hij deed dat heel langzaam en het mechanisme achter zijn nieuwe vermogen was nog steeds niet duidelijk. De onderzoekers van dit onderzoek wilden precies begrijpen wat er in de bacterie gebeurt als hij leert om zijn dieet te veranderen. Om hun vragen te beantwoorden, gebruikten ze een methode die ‘adaptieve laboratoriumevolutie’ (ALE) wordt genoemd.
Evolutie in een kolf
Eerst ontwikkelden de wetenschappers de bacterie door er extra stukjes DNA in te brengen via horizontale genoverdracht (HGT). Tijdens HGT neemt een bacterie DNA op dat vrij rondzweeft in de omgeving – in dit geval de reageerbuis. Deze stukjes DNA bevatten genen die afkomstig waren van verschillende soorten bacteriën die zich van nature kunnen voeden met xylose en dienden als instructies voor P. putida om dat ook te doen. Vervolgens gaven de onderzoekers deze gemanipuleerde bacterie xylose om zich mee te voeden en wachtten tot de bacterie erachter kwam hoe ze dat moest doen met de nieuwe instructies die ze had gekregen.
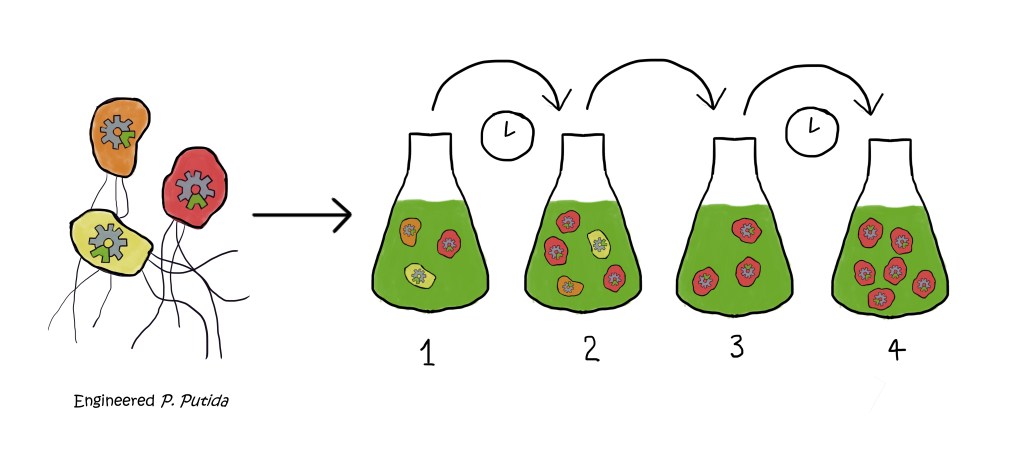
Vereenvoudigd diagram van adaptieve laboratoriumevolutie (ALE). 1. De gemanipuleerde bacteriën worden gekweekt in een medium met xylose. 2. Sommige groeien beter dan andere, wat betekent dat ze zich meer vermenigvuldigen. 3. Een deel van de bacteriën wordt overgeplaatst in een nieuwe kolf. De bacteriën die het goed doen en zich veel vermenigvuldigen, hebben een grotere kans om overgeplaatst te worden. 4. Na verloop van tijd zit de kolf vol met de gemanipuleerde bacterie die kan groeien op xylose. Afbeelding gemaakt door auteur met Krita 5.0.6.
Maar wanneer een bacterie een nieuw stukje DNA ontvangt, kan hij in het begin behoorlijk in de war zijn en heeft hij wat tijd nodig om zijn metabolisme opnieuw in te stellen. Sommige bacteriën kunnen het moeilijker hebben om eraan te wennen dan andere, en hier komt ‘survival of the fittest’ om de hoek kijken: sommige bacteriën kunnen willekeurig nieuwe mutaties verwerven die hen helpen te overleven in de nieuwe omgeving, of die hen helpen te wennen aan het nieuwe DNA-deel. Na verloop van tijd kunnen de bacteriën die zich beter kunnen aanpassen verder evolueren en zich vermenigvuldigen, en de perfecte bacterie worden voor het doel – zich voeden met xylose.
De onderzoekers gebruiken vervolgens andere laboratorium- en computermethoden om uit te zoeken wat er in deze geëvolueerde bacterie gebeurde toen deze werd gedwongen om zijn dieet om te schakelen van glucose naar xylose. Dit inzicht zal wetenschappers in de toekomst helpen om andere bacteriën sneller te leren van dieet te veranderen.
Link to the original post: Dvořák, P., Burýšková, B., Popelářová, B. et al. Synthetically-primed adaptation of Pseudomonas putida to a non-native substrate D-xylose. Nat Commun 15, 2666 (2024). https://doi.org/10.1038/s41467-024-46812-9
Featured image: Illustrated by Michaela Krupová using Krita 5.0.6
Vertaald door: Liang Hobma