Microbiologie in hapklare porties
Herpes en hersenen: Inzichten uit organoïde onderzoek
HSV, kort voor Herpes simplex virus, veroorzaakt de ziekte met dezelfde naam. Terwijl Herpes vaak wordt geassocieerd met zweertjes rond de mond of genitaliën, is het niet algemeen bekend dat het Herpes Simplex Virus hersenontsteking veroorzaakt (ontsteking van de hersenen met symptomen als aanvallen en hoofdpijn).
HSV-1, een van de twee subtypes van HSV, wordt behandeld met een antiviraal middel, acyclovir (ACV), dat helpt om de virale replicatie te stoppen. Veel mensen ervaren echter neurologische gevolgen na een HSV-1 infectie door schade aan neuronale processen en neuroepitheel.
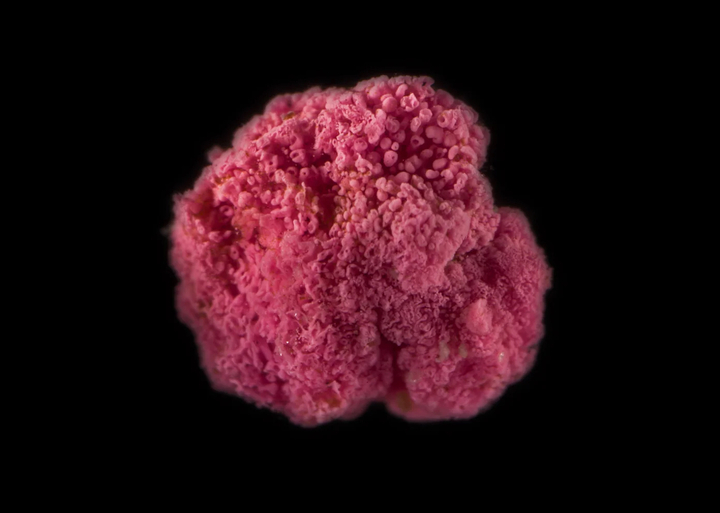
In dit onderzoek wilden Rybak-Wolf en hun team de progressie van HSV-1 beter begrijpen door gebruik te maken van cerebrale organoïden en de effecten van antivirale en ontstekingsremmende behandeling op de hersenschade veroorzaakt door HSV-1 infectie. Organoïden zijn in wezen vereenvoudigde versies van echte organen die zich enigszins als organen gedragen. Ze kunnen informeel tiny-brain, mini-liver enzovoort worden genoemd. Deze studie gaf inzicht in de associatie van HSV-1 met hersenweefsel.
HSV-1 infectie komt veel voor en treft een groot deel van de bevolking. HSV-1 verspreidt zich door nauw contact, zoals zoenen, terwijl het andere subtype, HSV-2, zich meestal verspreidt via seksueel contact. Dit onderzoek was gericht op het HSV-1 subtype omdat dit geassocieerd wordt met de meerderheid van herpes-geassocieerde encefalitis. HSV-1 infecteert voornamelijk epitheelcellen, maar het kan tientallen jaren sluimeren in het terminale gangliongebied van de hersenen totdat het wordt gereactiveerd door triggers zoals een verzwakte immuniteit en stresssignalen zoals blootstelling aan de zon, menstruatie, psychologische stress, koorts en operaties. Reactivering kan leiden tot de ontwikkeling van Herpes simplex encefalitis (HSE).
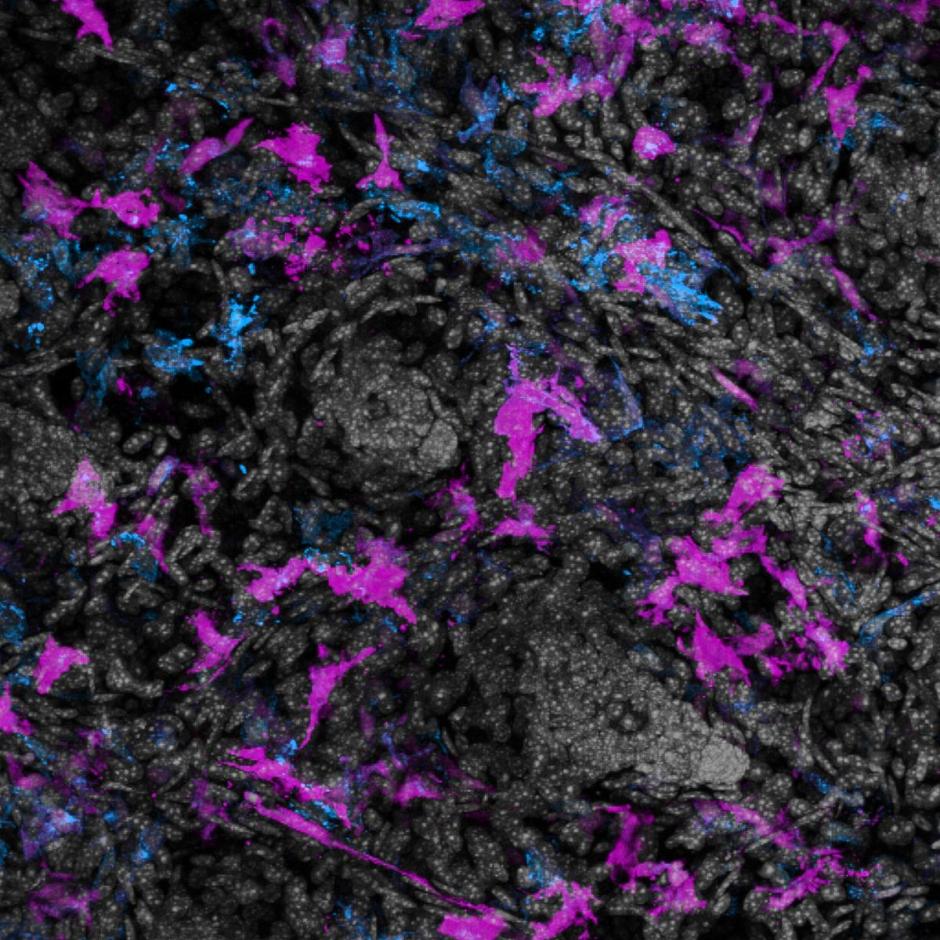
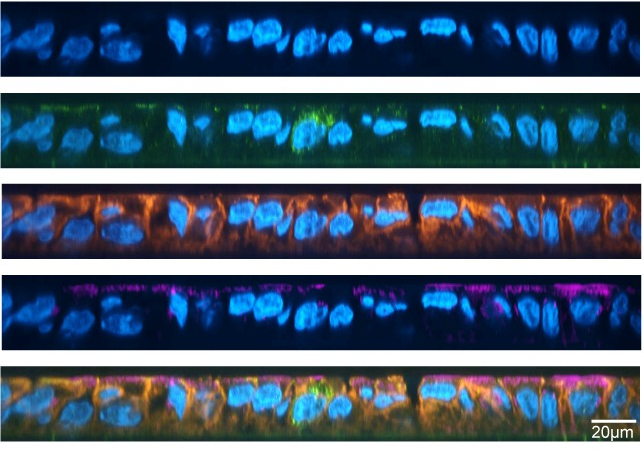
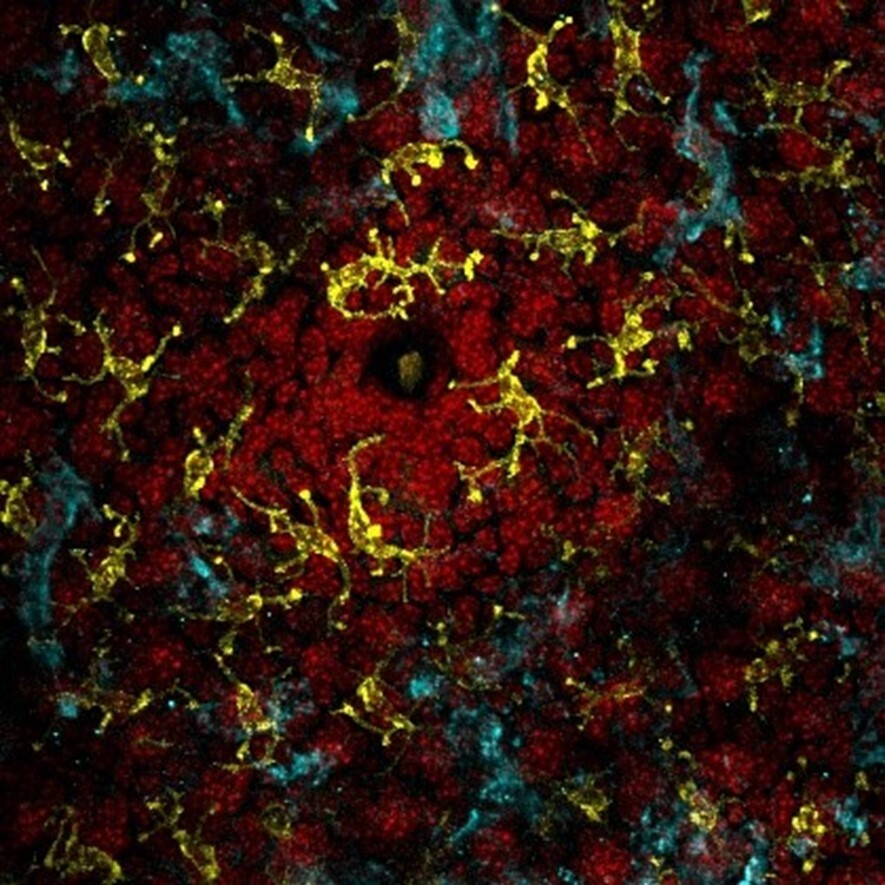
In het onderzoek werden menselijke hersenorganoïden gemaakt met behulp van geïnduceerde pluripotente stamcellijnen (iPS cellijnen), die de dorsale voorhersenen nabootsten. 60 dagen oude organoïden werden geïnfecteerd met een fluorescent proteïne-expresserende HIV-1-stam om de virale verspreiding in kaart te brengen en schade op cellulair en moleculair niveau te analyseren. Onderzoekers observeerden ook veranderingen in cellulaire identiteiten en expressie van verschillende genen en eiwitten (zoals SYN1 en HOMER1).
Daarnaast maten ze functionele aantasting, d.w.z. verlies van actieve neurieten, zoals werd geconcludeerd door beeldvorming van intracellulair calcium, aangezien calcium essentieel is voor de overdracht van signalen tussen neurieten. De resultaten van al deze tests en analyses wijzen erop dat HSV-1 beschadigingen op moleculair niveau, neuronale schade en snelle wijzigingen in de neuronale functie veroorzaakt. Onderzoekers concludeerden ook dat ontsteking veroorzaakt door de immuunrespons op HSV-1 infectie een rol speelt in de schade aan de hersenen.

Bron – Origineel artikel (met wijzigingen).
De TNF-signaleringsroute die geassocieerd is met de transcriptiefactor NF-κB was significant verhoogd. TNF is een cytokine, een soort signaalmolecuul dat een centrale rol speelt bij het reguleren van immuunreacties en ontstekingen, en NF-κB is een transcriptiefactor die de expressie regelt van vele genen die betrokken zijn bij immuunreacties, ontstekingen, overleving van cellen en andere cellulaire processen. TNF activeert verschillende eiwitten, waaronder kinases. Kinases activeren NF-κB om zich te binden aan specifieke plaatsen in het DNA. Dit leidt tot de productie van eiwitten die betrokken zijn bij ontstekingen, immuunreacties en het overleven van cellen. Kortom, ze zagen ontsteking van verschillende celtypen in de hersenorganoïden die werd veroorzaakt door TNF-signalering via NF-κB.

Onderzoekers analyseerden de effecten van het antivirale acyclovir (ACV) alleen en in combinatie met ontstekingsremmende medicijnen (necrostatine-1 en CDDO-Me). Ze stelden vast dat behandeling met acyclovir resulteerde in een significante afname van de HSV-1 replicatie, maar de ontsteking niet stopte. In tegenstelling hiermee verminderde een combinatorische behandeling van acyclovir en ontstekingsremmende medicijnen zoals necrostatine-1 of CDDO-Me effectief de ontsteking.
Dit onderzoek toont aan dat hersenorganoïden kunnen dienen als krachtige instrumenten om invasieve virussen te bestuderen en therapeutische behandelingen te modelleren. Beperkingen van hersenorganoïden zijn dat ze meer lijken op foetale hersenen dan op volwassen hersenen en dat ze immuuncellen en bloedvaten missen. Hoewel diermodellen en 2D culturen nuttig zijn en hun eigen voordelen hebben, zijn ze ook beperkt in hun mogelijkheden om effectief gebruikt te worden voor het modelleren van HSV-1.
We hopen dat in de toekomst complexere humane organoïden zullen worden gemaakt om dergelijke infecties beter te begrijpen.
Link to the original post:
Modelling viral encephalitis caused by herpes simplex virus 1 infection in cerebral organoids. Rybak-Wolf, A., Wyler, E., Pentimalli, T.M. et al. Modelling viral encephalitis caused by herpes simplex virus 1 infection in cerebral organoids. Nat Microbiol 8, 1252–1266 (2023). https://doi.org/10.1038/s41564-023-01405-y
Featured image: created by author using bing image creator and canva
Vertaald door: Liang Hobma