Microbiologie in hapklare porties
Bedraad voor schone energie: hoe unieke bacteriën elektriciteitsdraden maken
Geschreven door gastauteur Audrey Burnim
Wij vinden het vaak vanzelfsprekend dat een simpele druk op de knop een kamer kan verlichten, maar er is een gecompliceerd, zeer technisch proces voor de beweging van elektronen van energiebron naar gloeilamp. Onlangs hebben onderzoekers van de Universiteit van Yale onderzocht hoe een gewone bodembacterie, Geobacter genaamd, elektriciteit kan produceren met behulp van eiwitten en metaalionen. Dit unieke vermogen stelt hen in staat te gedijen in omgevingen met weinig zuurstof, zoals vervuilde bodems en sedimenten. Een van de belangrijkste onderdelen van dit elektronenoverdrachtsproces is de vorming van nanodraden, die dienen als geleidende bruggen voor de overdracht van elektronen van de bacterie naar externe elektronenacceptoren.
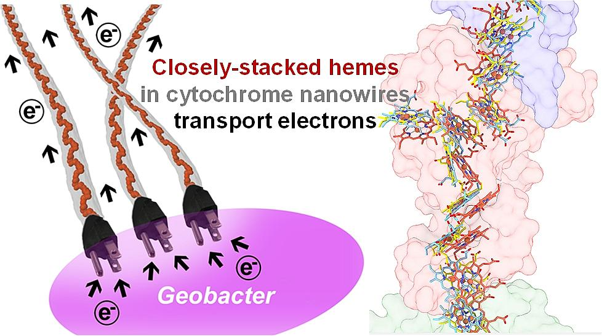
Onderzoekers zijn geïnteresseerd in deze familie van bacteriën vanwege hun unieke vermogen om zonder zuurstof te overleven en methaan te eten. Fascinerend is dat het metabolisme van de bacteriën ook elektronen buiten hun cellen verplaatst, waarbij elektrische energie wordt geproduceerd in een proces dat bekend staat als extracellulair elektronentransport. Methaan is een belangrijke veroorzaker van broeikasgassen die de klimaatverandering snel versnellen, dus deze bacteriën kunnen een potentiële oplossing zijn voor het opwekken van energie en het verbeteren van de klimaatcrisis [1]. Hoe deze eiwitten hun eigen machinerie organiseren op een manier die de vorming van een moleculaire draad mogelijk maakt, waarbij elektronen efficiënt worden vervoerd – net als bij draden die wij gebruiken – was grotendeels een mysterie tot dit werk van Yangqi Gu en medewerkers. Een langetermijndoel van dit onderzoek op moleculair niveau is dat wetenschappers het metabolisme van deze microben op een dieper niveau kunnen begrijpen om bacteriën te ontwikkelen die efficiënter methaan eten.
In dit recente artikel in Nature Microbiology genaamd “Structure of Geobacter cytochrome OmcZ identifies mechanism of nanowire assembly and conductivity,” gebruikten de onderzoekers cryogene elektronenmicroscopie (Cryo-EM) en andere experimenten om te kijken hoe Geobacter sulfurreducens CL-1 deze draden op moleculair niveau maakt en hoe ze elektrische stroom opwekken. Zij ontdekten dat deze nanodraden werden gemaakt door metaalhoudende moleculen, heemverbindingen genaamd, nauwkeurig te rangschikken. Deze moleculen bevatten ijzer (Fe) in het midden. Ons lichaam verplaatst ijzer en zuurstof met behulp van dezelfde heemverbindingen, en zij maken ons bloed rood [2]! Deze heemmoleculen worden precies op hun plaats gehouden door eiwitten die “OmcZ” worden genoemd. OmcZ wordt geclassificeerd als een cytochroom, wat letterlijk “celpigment” betekent, omdat de structuren een karakteristieke reeks waarneembare kleuren hebben, gebaseerd op hoe de molecule licht absorbeert.
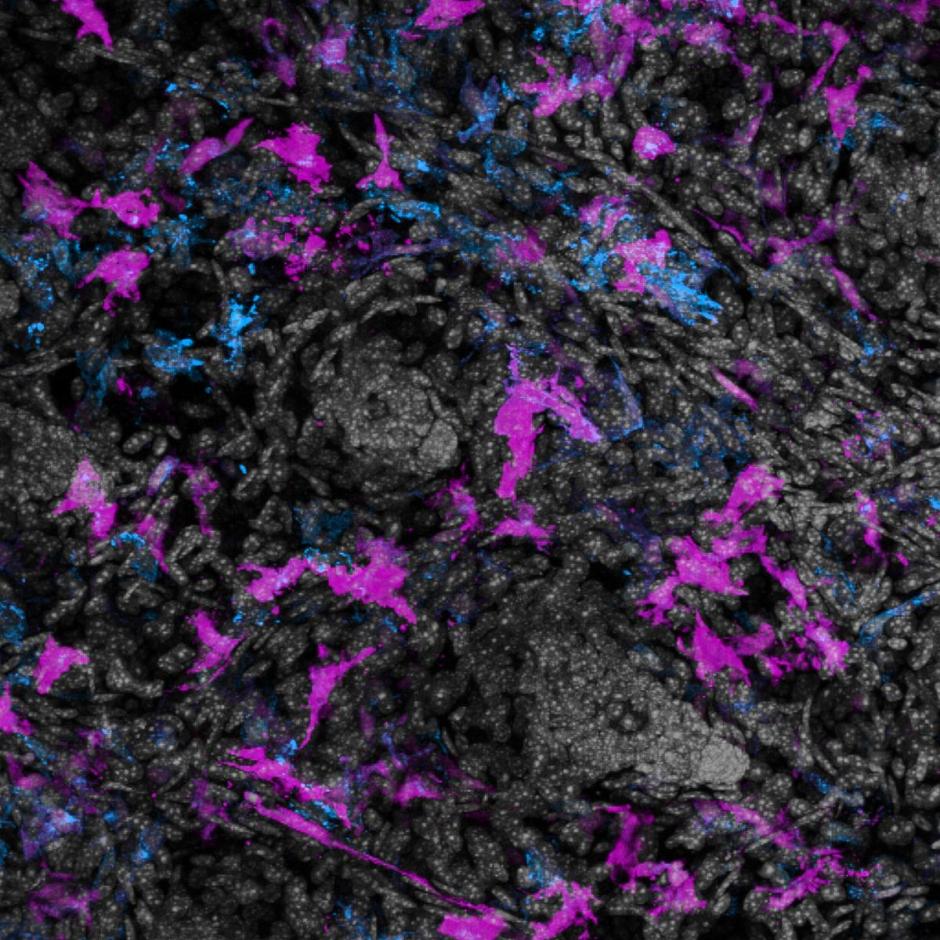
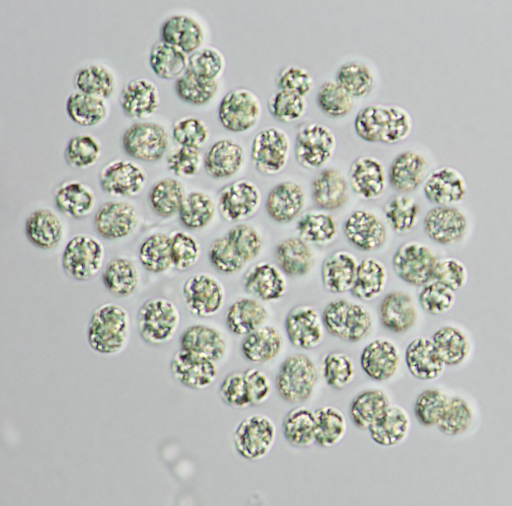
De onderzoekers ontdekten dat OmcZ het enige eiwit is dat essentieel is voor de vorming van elektrische stroom in Geobacter sulfurreducens biofilms. Biofilms verwijzen naar de manier waarop Geobacter sulfurreducens met elkaar interageren [3,4]. Ze vormen grote aggregaten en matrices van hun cellen en extracellulaire componenten, in dit geval een groot complex van nanodraden. De dichtheid van G. sulfurreducens in de biofilm was zeer hoog, wat bijdroeg tot de grote hoeveelheid waargenomen elektriciteit.
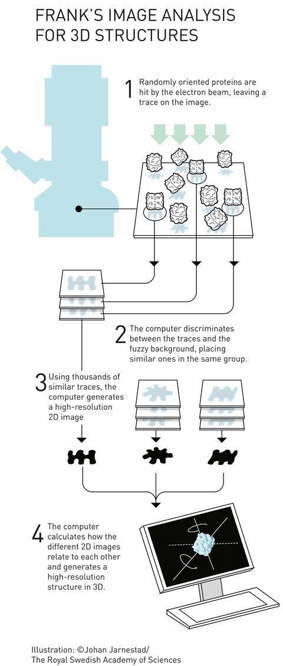
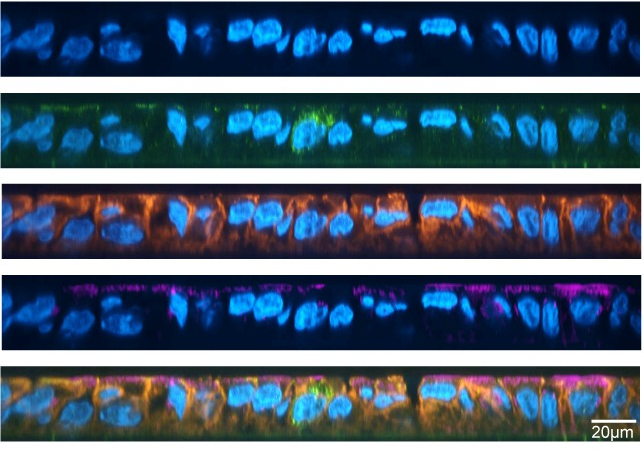
Cryogene elektronenmicroscopie (cryo-EM) werd gebruikt om deze nanodraden zichtbaar te maken. Cryo-EM is een krachtige en Nobelprijswinnende [5] beeldvormingstechniek waarmee onderzoekers monsters van eiwitten kunnen nemen, er elektronen op afvuren en reconstrueren hoe hun elektronendichtheid eruit ziet, zodat een 3D-moleculair model kan worden opgebouwd. Hieronder volgt een vereenvoudigde weergave van een voorbeeldworkflow.
Het 3D-model dat uit dit werk resulteerde (links in de figuur aan het begin van dit artikel) gaf een gedetailleerd beeld van hoe individuele stukjes van deze nanodraad zijn opgebouwd.
Bovendien ontdekten de onderzoekers dat de organisatie van het nanodraadnetwerk zich kan herschikken in verschillende biochemische omgevingen, wat wijst op het aanpassingsvermogen van OmcZ-nanodraden aan verschillende omstandigheden. Deze veelzijdigheid kan verklaren waarom Geobacter-soorten kunnen gedijen in diverse omgevingen met verschillende elektronenacceptoren.
Naast de structurele bevindingen ontdekten de onderzoekers ook de rol van een serineprotease, een soort enzym, bij het regelen van de assemblage van OmcZ-monomeren tot nanodraden. Dit protease bleek cruciaal te zijn bij het regelen van de vorming en stabiliteit van OmcZ-nanodraden. Deze ontdekking biedt inzicht in de ingewikkelde mechanismen die ten grondslag liggen aan de assemblage van OmcZ-nanodraden en werpt een licht op de complexe wisselwerking tussen eiwitten bij de vorming van deze geleidende structuren.
Fascinerend is dat de onderzoekers ontdekten dat zowel OmcZ als het serineprotease wijdverbreid zijn in belangrijke bacteriën en archaea, wat erop wijst dat de biogenese van nanodraden een wijdverbreid fenomeen kan zijn in verschillende soorten en omgevingen. Dit onderstreept het belang van OmcZ-nanodraden in de microbiële wereld en hun mogelijke implicaties voor milieuprocessen, zoals bioremediëring en energieproductie.
De bevindingen van deze studie hebben nieuwe mogelijkheden geopend voor het begrijpen van de fundamentele mechanismen van elektronenoverdracht in bacteriën en de potentiële toepassingen van OmcZ-nanodraden op verschillende gebieden. De hoge elektronengeleiding en het aanpassingsvermogen van OmcZ-nanodraden maken ze tot een veelbelovende kandidaat voor bio-elektronische apparaten, zoals biobrandstofcellen en biosensoren. De wijdverbreide aanwezigheid van OmcZ en het serineprotease in diverse bacteriële soorten suggereert dat de biogenese van nanodraden een gebruikelijke strategie is die bacteriën gebruiken voor extracellulair elektronentransport.
Link to the original post: Gu, Y., Guberman-Pfeffer, M.J., Srikanth, V. et al. Structure of Geobacter cytochrome OmcZ identifies mechanism of nanowire assembly and conductivity. Nat Microbiol 8, 284–298 (2023). https://doi.org/10.1038/s41564-022-01315-5
Featured image: Protein Nanowire Lab, Yale University.
(1) What is the greenhouse effect?. Climate Change: Vital Signs of the Planet. https://climate.nasa.gov/faq/19/what-is-the-greenhouse-effect/ (accessed 2023-04-28).
(2) Lichtin, A. Does Blood Turn Blue?. Cleveland Clinic. https://health.clevelandclinic.org/what-color-is-blood/ (accessed 2023-04-28).
(3) Biofilm. https://doi.org/10.1016/B978-0-323-85146-6.00020-6.
(4) Donlan, R. M. Biofilms: Microbial Life on Surfaces. Emerg. Infect. Dis. 2002, 8 (9), 881–890. https://doi.org/10.3201/eid0809.020063.(5) The Nobel Prize in Chemistry 2017. Nobelprize.org. https://www.nobelprize.org/prizes/chemistry/2017/press-release/ (accessed 2023-04-28).
Vertaald door: Liang Hobma