Microbiologie in hapklare porties
Acne, antibiotica en zwakke botten
Stel je voor dat je in een achtbaan stapt – de spanning, de bloedstoot en de angst. Het kan een van de meest levendige ervaringen zijn die in je geheugen gegrift staan. Maar soms gaat die kick ook gepaard met een golf van ongewenste en nogal gênante misselijkheid. Deze misselijkheid is wat acne voelt als een puberale achtbaan. Deze kleine uitdagende plekjes, veroorzaakt door de verstopping van de haarzakjes door dode huid en talg (een olieachtige substantie die de huid beschermt tegen uitdroging), zijn de dermale synoniemen voor een nachtmerrie.
Acne is een veel voorkomende huidaandoening die ongeveer 85% van de adolescenten en jongvolwassenen treft. Wanneer topische behandelingen niet werken, worden antibiotica voorgeschreven om de huid te zuiveren. Ongeveer 40% van deze patiënten krijgt minocycline toegediend. Minocycline is een antibioticum op basis van tetracycline dat wordt gebruikt om bacteriële infecties in verschillende lichaamsdelen te behandelen. Minocycline vermindert ontstekingen en roodheid, waardoor de gevolgen van acne worden afgezwakt. De gemiddelde duur van deze specifieke antibioticakuur varieert van 4 tot 11 maanden.
Volgens een recente studie, gepubliceerd in het Journal of Clinical Investigation (JCI), is het langdurig gebruik van deze antibiotica schadelijk voor het darmmicrobioom. Het darmmicrobioom is een groep microben die de darm koloniseren. Enkele bekende voorbeelden van darmbacteriën zijn Helicobacter pylori, E. coli en Lactobacillus. De interacties tussen de gastheer en deze microben beïnvloeden de ontwikkeling en de homeostase van de weefsels van de gastheer, zowel lokaal in de darm als op afgelegen extra-gastro-intestinale plaatsen (plaatsen buiten de darm). De darmbacteriën helpen bij de spijsvertering en de regulering van het immuunsysteem, bieden bescherming tegen andere ziekteveroorzakende bacteriën, produceren vitaminen zoals vitamine B12, riboflavine enz. en regelen ook de werking van botcellen.
Antibiotica veroorzaken veranderingen in de inheemse darmbacteriën, waardoor het darmmicrobioom uit balans raakt. Deze toestand wordt dysbiose genoemd. De veerkracht van de darmmicrobiota om te herstellen van door antibiotica veroorzaakte dysbiose wordt aangetast door de toediening van antibiotica tijdens kritieke ontwikkelingsfasen (zoals de adolescentie) en uitgebreide antibioticakuren. Wetenschappelijke studies tonen aan dat ongeveer 40-50% van de totale botmassaopbouw (toename van de botmassa) plaatsvindt tijdens de adolescentie.
HOE HET DARMMICROBIOOM DE GEZONDHEID VAN DE BOTTEN BEÏNVLOEDT:
Om het verband tussen het darmmicrobioom en de gezondheid van de botten te begrijpen, moeten we eerst hun wederzijdse vriend begrijpen: de galzuren. Galzuren zijn moleculen die door de lever worden gesynthetiseerd. Ze zijn verantwoordelijk voor de opname van vetmoleculen en in vet oplosbare vitaminen zoals vitamine D, een cruciaal onderdeel van de botvorming en calciumopname.
En raad eens wie dit hele vetoplossingskartel leidt? Het is onze eigen gal; wat betekent dat elke onbalans in de galzuurniveaus in het lichaam leidt tot problemen met de absorptie van vitamine D. Nu we weten hoe de galzuren verband houden met de gezondheid van de botten, laten we begrijpen hoe ze samenwerken met het darmmicrobioom.
Normaal zet de darmmicrobiota in de darm primaire galzuren – geproduceerd in de lever – om in secundaire galzuren. De galzure homeostase (evenwicht) in het hele lichaam wordt geregeld door een darm-lever endocriene as (een communicatienetwerk dat de darm-, lever- en centrale zenuwstelsels verbindt) die FXR- FGF 15 heet. Verstoringen in de werking van deze as leiden tot een onevenwicht in de circulerende galzuurniveaus in het lichaam.
Bovendien beïnvloeden de galzuren ook oppervlakte-intestinale receptoren zoals FXR (farnesoid X receptor) door ze te activeren of te deactiveren. Activering van FXR produceert het hormoon FGF19, dat werkt als een signaalmolecuul. Met behulp van hepatocyte-fibroblast groeifactor receptor 4 (FGFR4) onderdrukt FGF19 de synthese van galzuren uit de lever en handhaaft het gezonde galzuurniveaus in het lichaam.
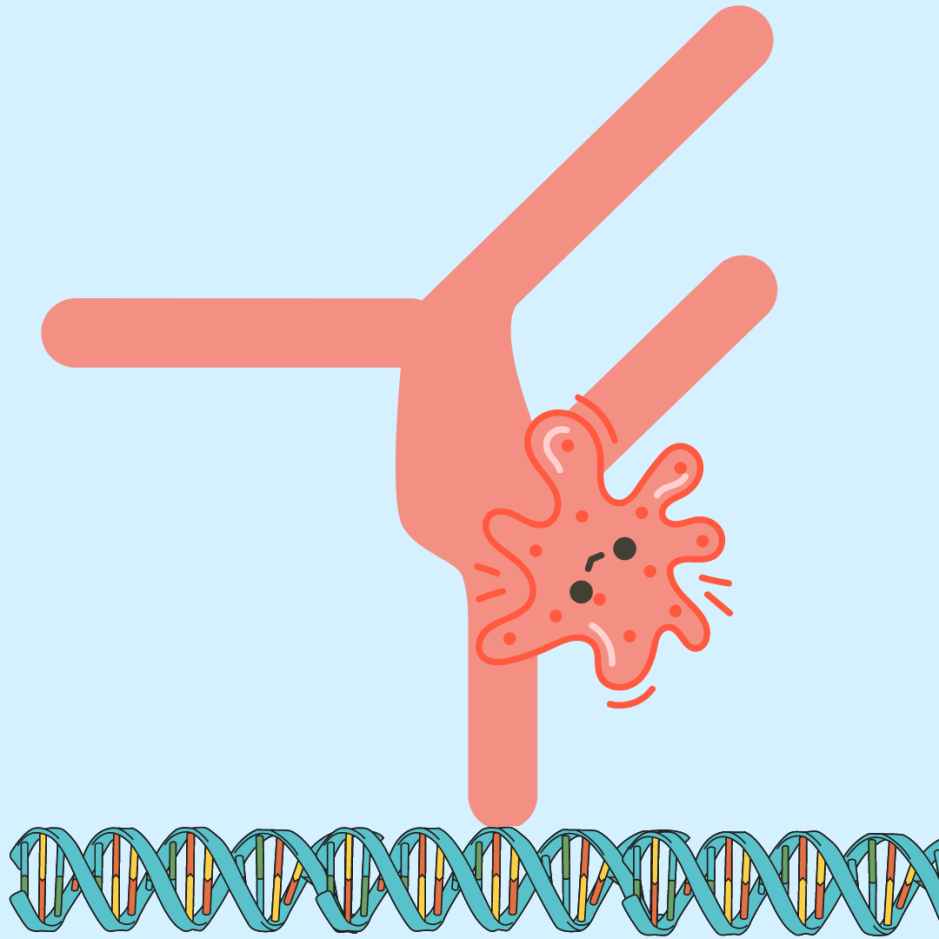
Daarom veranderen veranderingen in de samenstelling van de darmbacteriële gemeenschappen na toediening van antibiotica voor de behandeling van acne, de intestinale microbiële biotransformatie van galzuren, en zoals hierboven uiteengezet, beïnvloeden zij het skelet via de opname van vitamine D (figuur 1).
STUDIEONTWIKKELING:
Er werd een experiment uitgevoerd op mannelijke en vrouwelijke testmuizen om de effecten van minocycline op het darmmicrobioom te bestuderen. Muizen bereiken de puberteit met ongeveer 5 tot 6 weken en de botontwikkeling is voltooid in 12 weken. In de studie kregen beide geslachten minocycline toegediend vanaf de leeftijd van 6 tot 12 weken.
De mannelijke muizen werden op 12 weken geëuthanaseerd om na te gaan of de effecten van minocycline op de skeletrijping afhangen van de darmmicrobiota.
De vrouwelijke muizen werden geëuthanaseerd op de leeftijd van 12 en 18 weken, om geslachtsverschillen en de effecten van onmiddellijke en langdurige antibioticabehandeling te evalueren.
DE BELANGRIJKSTE CONCLUSIES VAN DEZE EXPERIMENTEN:
De diversiteit van het darmmicrobioom verminderde met 60% na toediening van minocycline. Deze veranderingen waren echter geslachtsafhankelijk, waarbij de vrouwtjes een upregulatie van bepaalde bacteriesoorten vertoonden en de onderdrukking van sommige andere. Bij mannen werd echter geen toename van het aantal bacteriesoorten waargenomen. Deze veranderingen werden toegeschreven aan de verschillen in geslachtshormonen tussen beide geslachten.
FGF 19, dat betrokken is bij het behoud van de botmineraaldichtheid, werd in lage niveaus aangetroffen bij vrouwelijke testmuizen. Hieruit werd afgeleid dat lage niveaus van FGF 19 de botten negatief kunnen beïnvloeden.
Ten slotte werd aangetoond dat minocycline de vorming van osteoclasten, de botafbrekende cellen, bevordert, terwijl het de vorming van osteoblasten, de botsynthetiserende cellen, onderdrukt.
Link to the original post: Matthew D. Carson, Amy J. Warner, Jessica D. Hathaway-Schrader, Vincenza L. Geiser, Joseph D. Kim, Joy E. Gerasco, William D. Hill, John J. Lemasters, Alexander V. Alekseyenko, Yongren Wu, Hai Yao, Jose I. Aguirre, Caroline Westwater, Chad M. Novince. Minocycline-induced disruption of the intestinal FXR-FGF15 axis impairs osteogenesis in mice. JCI Insight, 2022; DOI: 10.1172/jci.insight.160578
Featured image: https://www.craiyon.com
Vertaald door: Liang Hobma